Низкотемпературная переработка природного газа
ГЛАВА XV
НИЗКОТЕМПЕРАТУРНАЯ ПЕРЕРАБОТКА ПРИРОДНОГО ГАЗА
В 20-х годах прошлого столетия Хемфри Дэви, Майкл Фарадей, М. Наттерер, Каньяр де ля Тур (Humphry Davy, Michael Faraday, M. Natterer, Cagnard de la Tour) и другие европейские ученые установили, что все обычные газы можно привести в жидкое состояние и что при повышении температуры смеси газ — жидкость в них происходят критические явления [1.9]. К 1900 г. удалось перевести в жидкое состояние водород и гелий и после этого утвердилось представление о том, что все вещества могут существовать в газообразном, жидком и твердом состояниях. Критическая температура метана равна —82,5° С, при обычном давлении он кипит при температуре —161,5° С. Возможности осуществления технологических процессов при столь низких температурах ограничены, но для специальных целей их использование является целесообразным (например, производство жидкого кислорода) '. Опыт этого производства представляет ценность и для других низкотемпературных процессов [XV. 4, XV. 22].
К низкотемпературным можно отнести процессы выделения из природного газа этана, азота, гелия, сжиженных газов и конденсата.
§ 1. РАВНОВЕСНЫЕ СООТНОШЕНИЯ МЕЖДУ ФАЗАМИ
В главе III рассматривалось фазовое поведение систем метан — этан [III. 8] и метан — азот [111.7,111.15]. Следует отметить, что максимальное абсолютное давление двухфазной системы метан — этан равно 70 ат (рис. III. 11). Эта цифра типична для максимального давления двухфазных углеводородных систем при низкой температуре. Следовательно, для низкотемпературных процессов характерно среднее давление. Уровень максимального давления двухфазных систем определяется в основном близостью температур кипения компонентов, входящих в смесь, ибо при добавлении водорода к системам, состоящим из легких углеводородов, двухфазная область существует при абсолютном давлении 560, 700 ат и больше [XV. 3, XV. 5, XV. 6, XV. 36]. Имеющиеся данные о равновесии пар — жидкость для систем, находящихся при низкой температуре, обобщены в работе Руэмана (Ruhemann) [XV. 27].
Следует отметить, что все летучие углеводороды замерзают при температуре около—185°С (табл. IV. 1). Чистый метан замерзает при температуре —182,5° С. Наинизшую температуру замерзания имеет пропан:
— 187,6° С; этилен замерзает при —167,6° С и я-бутан при —138,3° С. Хотя под действием давления растворенных водорода или азота можно снизить температуру замерзания углеводородов, но при абсолютных давлениях порядка 140—210 ат это влияние незначительно.
Характеристика системы метан — этан, уже показанная наряду с системой азот — метан на рис. III. 10, представляет фазовые соотношения, имеющие большое значение для низкотемпературной переработки природного газа. На рис. XV. 1 приведена плотность насыщенных паров и жидкостей в смеси метан — этан. Константы равновесия для этой системы приведены в табл. XV. 1.
Система азот — метан была исследована Блумером и Перентом (Bloomer and Parent) [III. 7], а также Сайнсом, Роучем, Хогеном и Ролендом (Cines, Roach, Hagan and Roland) [III. 15]. Диаграммы этой системы показаны на рис. XV. 2 — XV. 6. Данные, полученные Сайнсом и другими, близки к данным Филипса (Philips) и Института газовой технологии (рис. XV. 7) [III. 8]. Описанию свойств азота при низких температурах посвящена работа Блумера и Pao (Bloomer and Rao) [XV. 7]. Диаграммы Моллье (Mollier) для азота и метана приведены на рис. XV. 8 и XV. 9. Кривая энтальпия— состав для смеси метан — азот показана на рис. XV. 10 [XV. 8].
Поведение системы двуокись углерода — метан представляет интерес, поскольку характеризует равновесные условия существования паровой, жидкой и твердой фаз. Фазовое поведение этой системы рассмотрено в работе Доннелли и Катца (Donnely and Katz). На рис. XV. 11 и XV. 12 показаны условия перехода смеси пара и жидкой фазы в смесь пара и твердой фазы. Как следует из этих кривых, метан снижает температуру замерзания двуокиси углерода.
При малом содержании С02 твердая фаза не образуется. При охлаждении природного газа, содержащего около 1,5% СОг, вплоть до температуры сжижения метана трудностей, связанных с образованием твердой фазы, может не встретиться.
1 Сейчас начинают использовать производство жидкого метана с последующей транспортировкой его в жидком состоянии в специальных танкерах. — Прим. ред.
Величины К в системе метан — этан. Величины К для метана
[III. 8]
| Температура, °С | Абсолютное давление, ат | ||||||||
| 7 |
14 | 21 | 28 |
35 | 42 | 49 |
56 | 63 | |
| ¦ | —205,5 | — 178,2 |
— 159,5 | — 145,2 |
—132,9 | — 122,5 |
—110,5*** | —88,4*** |
—62,4 |
| —128,9 |
1,16 | ||||||||
| — 117,8 | 2,02 | ||||||||
|
— 106,7 | 2,99 | 1,44 | |||||||
| —95,6 | 4,06 | 2,01 | 1,36 |
1,06 | |||||
| —84,4 | 5,45 |
2,68 | 1,82 | 1,38 |
1,13 | 1,02 | |||
| —73,3 | 6,95 | 3,33 | 2,28 |
1,76 | 1,42 | 1,20 |
1,06 | ||
|
—62,2 | 8,61 | 4,02 |
2,73 | 2,10 | 1,71 | 1,43 | 1,24 |
1,09 | |
| —51,1 |
9,78 | 4,85 | 3,17 | 2,43 | 1,97 |
1,67 | 1,44 | 1,28 |
1,08 |
| —40,0 |
_ | 5,64 | 3,66 |
2,73 | 2,20 | 1,86 | 1,62 | 1,42 |
1,23 |
| — 28,9 |
— | 6,23 | 4,16 |
3,05 | 2,40 | 2,00 | 1,74 | 1,52 |
1,33 |
| —17,8 |
_ | _ | 4,46 |
3,37 | 2,63 | 2,18 |
1,87 | 1,59 | 1,39 |
| —6,6 | _ |
— | — | 3,54 | 2,83 | 2,30 |
1,91 | 1,63 | 1,30 |
| 4,4 | _ |
_ | _ | 3,62 |
2,85 | 2,36 | 1,91 |
1,63 | 1,23 |
|
15,6 | — | — |
— | — | — | 2,30 | 1,82 | ||
| 26,7 | _ |
_ | _ | _ |
— | — | 1,61 | ||
| *« |
—46,0 | —6,2 | 21,6 | 43,0 | 61,0 |
75,8 | 88,3 | 72,6*** |
48.3*** |
Величина К для этана
| —205,5 | — 178,2 |
—159,5 | — 145,2 |
—132,9 | —122,5 |
—110,5*** | —88,4*** |
—62,4*** |
| 0,00735 |
||||||||
| 0,0350 | ||||||||
| 0,0710 | 0,0540 | |||||||
| 0,1291 | 0,0925 | 0,0890 | 0,1148 | |||||
|
0,2225 | 0,1446 | 0,1257 | 0,1349 | 0,1712 |
0,2438 | |||
|
0,3550 | 0,2213 | 0,1822 | 0,1735 | 0,193 |
0,2515 | 0,398 | ||
| 0,546 | 0,3265 |
0,264 | 0,2372 | 0,240 | 0,275 | 0,339 |
0,5645 | |
| 0,798 |
0,4571 | 0,363 |
0,3255 | 0,3115 | 0,322 | 0,358 | 0,441 |
0,718 |
| 0,631 |
0,4798 | 0,421 | 0,405 | 0,405 | 0,421 |
0,462 | 0,583 | |
|
_ | 0,839 | 0,6237 |
0,540 | 0,510 | 0,497 | 0,506 | 0,533 |
0,619 |
| 0,7975 | 0,674 | 0,6175 |
0,596 | 0,5975 | 0,612 | 0,680 | ||
| _ | _ | 0,815 |
0,739 | 0,703 | 0,6875 | 0,708 | 0,760 | |
| _ | _ |
0,980 | 0,873 | 0,814 |
0,790 | 0,807 |
0,894 | |
| _ | _ | 0,995 |
0,926 | 0,881 | 0,929 |
|||
| _ |
__ | _ | .— |
0,985 | ||||
|
—46,0 | —6,2 | 21,6 | 43,0 | 61,0 |
75,8 | 88,3 | 72,6*** |
48,3*** |
Критическая температура смеси.
Температура насыщения метана, *• Температура насыщения этана.
— 128,9
— 117,8
— 106,7 —95,6 —84,4 —73,3 —62,2 —51,1 —40,0 —28,9 —17,8
—6,6
4,4
15.6
26.7
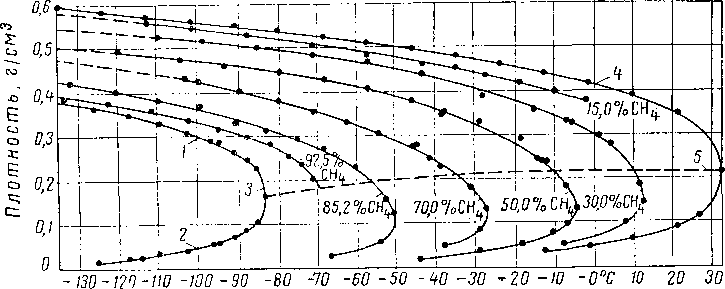
Рис. XV. 1. Плотность насыщенных паров и жидкостей в смеси метан — этан [111.8]. / — насыщенная жидкость; 2 — насыщенный пар; 3 — чистый метай; 4 — чистый этан; 5 —приближенное геометрическое место точек критический плотности.
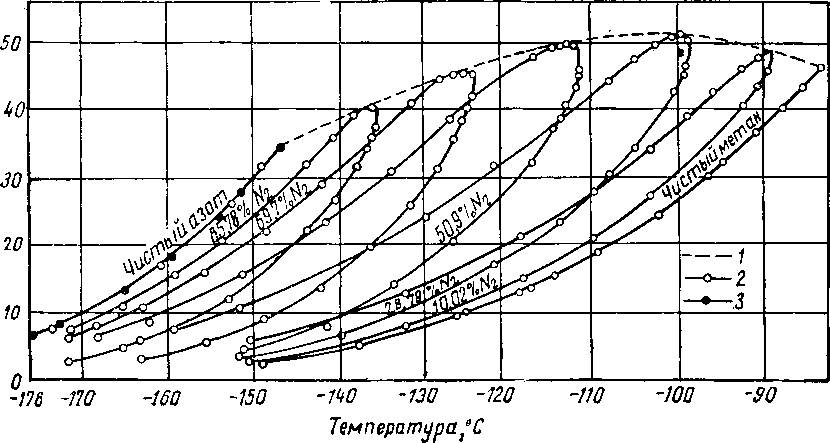
Рис. XV. 2. Диаграммы температур точек росы и начала кипения длясистемы метан—азот [III. 7]. / —I геометрическое место критических точек; 2 — измерения Института газовой технологии; 3 — критические
гочки по международным таблицам.
Абсолютное давление, atn
|
гЧ9ат | |||||||||
| \ | |||||||||
| 42 | |||||||||
|
\ | 1 |
||||||||
| \ | j | 28 | |||||||
| '21 |
|||||||||
| "Ъ~ | -V- | \ |
s\ | п | |||||
| |\ |
м | 7 | |||||||
| ^1 ГГ*4 | к |
||||||||
| \| | J | ||||||||
| |\ | |||||||||
| 1 | к | ||||||||
| 1 |
1 Со'стаЬ | пара | ||||||||
|
ъ жиг | стао тсгг | X | |||||||
| —Г— 1 |
\4 | X | |||||||
|
1 I | 1 | / |
\ | ||||||
| 1 Г | |||||||||
Состав, мольная концентрация азота
-55< •90, -95 -100 -105 -110 -115 ^-120 gi-W
I- -ы
с; _
? '
.и
^ -т
-145
-¦iso
-155
-160
¦165
-110
-175
Рис. XV. 3. Диаграмма зависимости состава от изобарной температуры для системы метан — азот [III. 7].
Равновесные составы жидкости и пара определены при —123° С и абсолютном давлении, равном 14 ат.
Плотность, г/ см
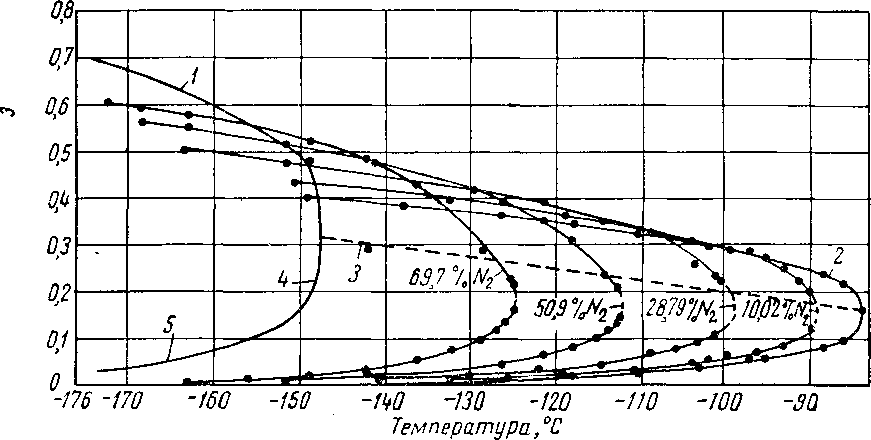
Рис. XV. 4. Плотность насыщенных паров и жидкости в системе метан — азот [III. 7].
/ — насыщенная жидкость; 2— чистый метан; 3 — геометрическое место критических точек; 4 —
чистый азот; 5 — насыщенный пар.
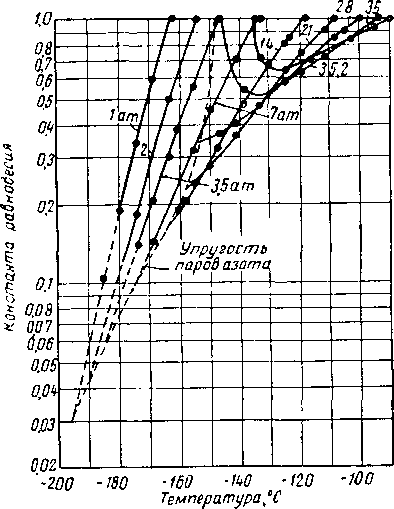
Рис. XV. 5. Константы равновесия для метана в системе метан — азот [III. 7].
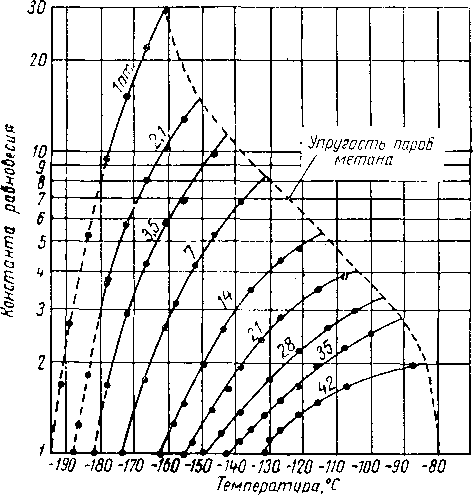
Рис. XV. 6. Константы равновесия для азота в си стеме метан — азот [III. 7].
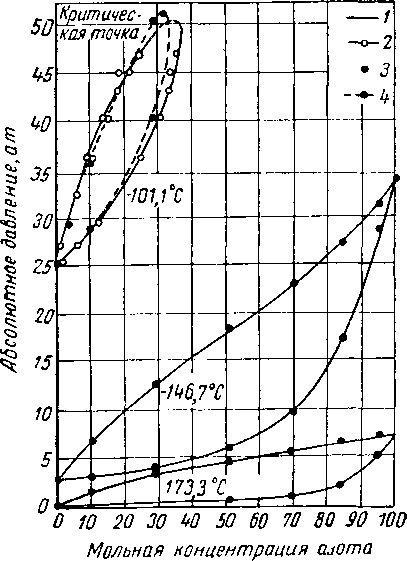
Рис. XV. 7. Сопоставление экспериментальных данных Сайнса с данными Института газовой технологии [III. 8].
I — сглаженная линия Сайнса и др.; 2 — экспериментальные данные Сайнса н др.; 3 — экспериментальные данные Института газовой технологии; 4 — сглаженные данные Института газовой технологии при —101° С.
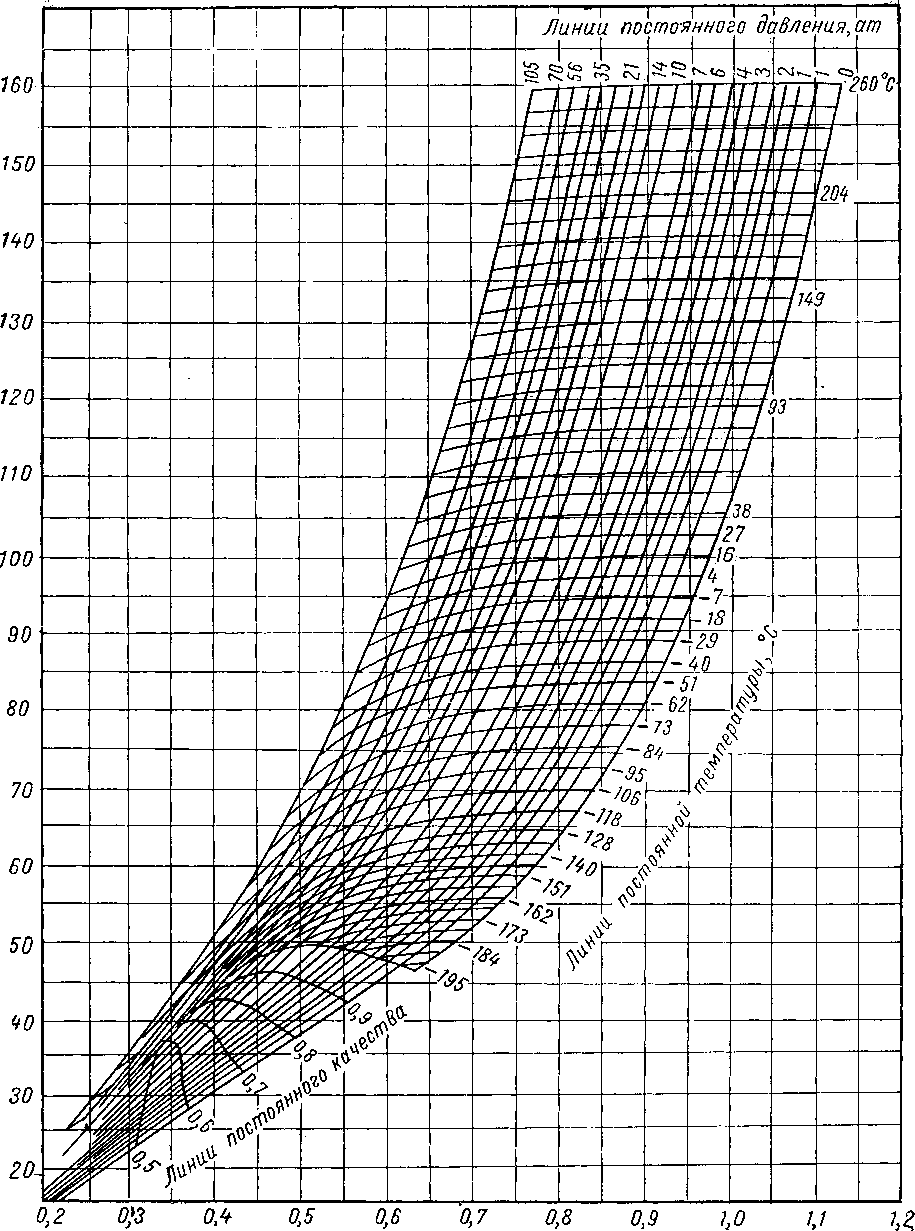
Э н т альпия, ккал/кг
Рис. XV. 8. Диаграмма Моллье для азота [XV. 7].
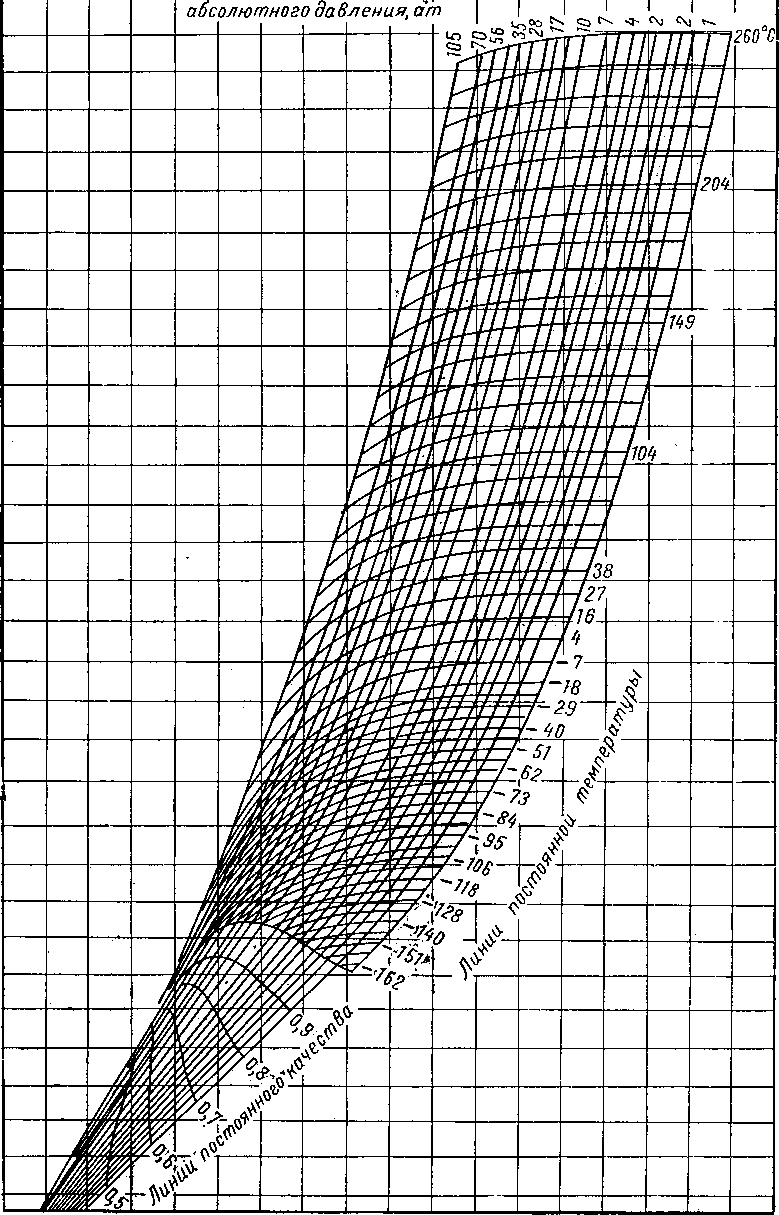
Энтальпия, нкал/кз
О ----------
О 10 20 30 UO 50 60 10 80 S0100 Составу мольная концентрация азота
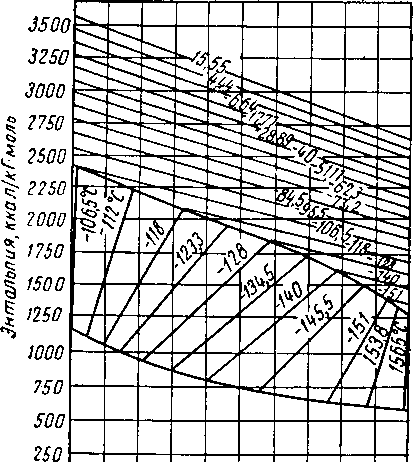
Рис. XV. 10. Диаграмма зависимости энтальпии от состава для смесей метан — азот при абсолютном давлении 21 ат [XV. 8].
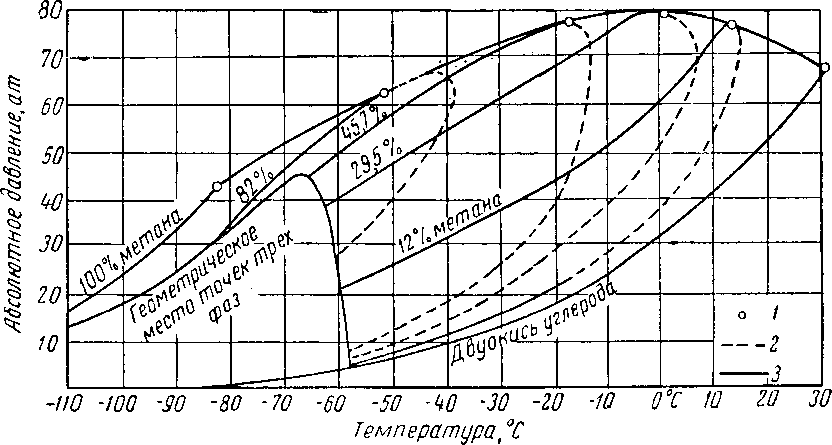
Рис. XV. 11. Диаграмма зависимости давления or температуры для системы двуокись углерода — метан [XV. 15].
/—^критические точки; 2 — точки росы; 3 — точки начала кипения.
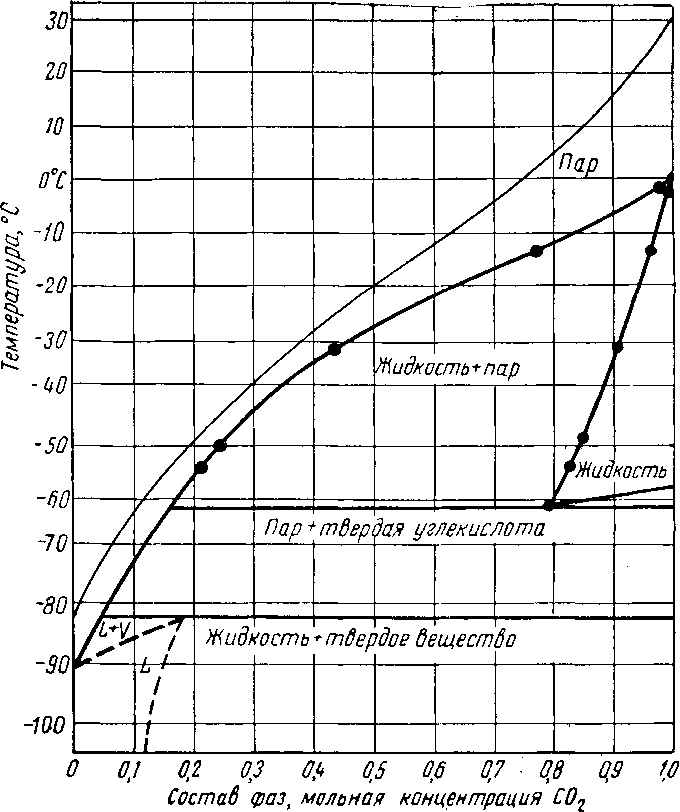
Рис. XV. 12. Диаграмма зависимости состава системы двуокись углерода — метан от температуры прн абсолютном давлении 35 am [XV. 15].
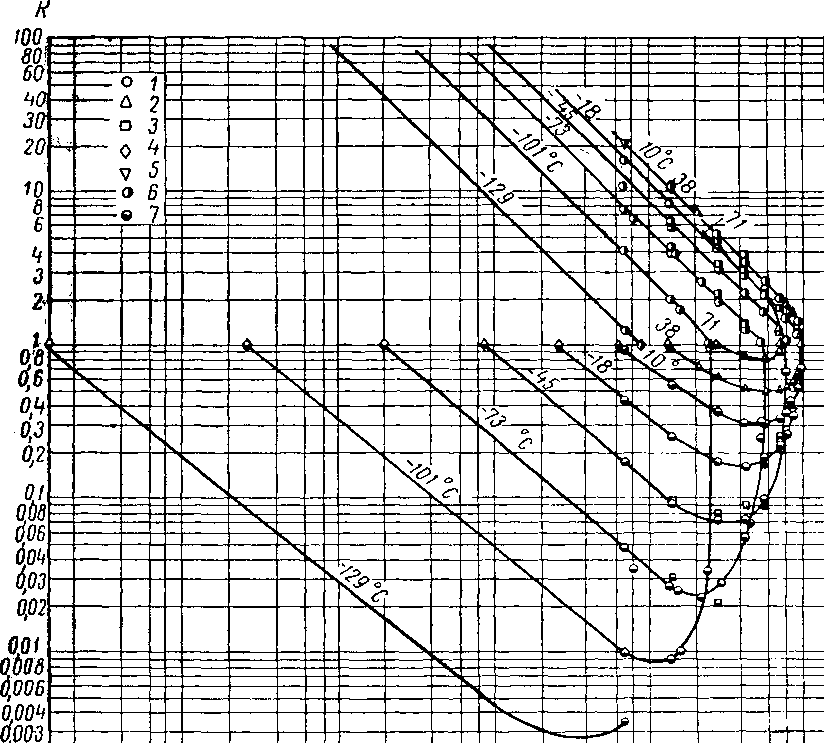
Фазовое поведение системы метан — этан — пропан и связанных с нею двойных смесей при низких температурах и различных давлениях, вплоть до критических для данных смесей, было изучено Прайсом (Prise) ,[XV. 26а]. Этими данными можно воспользоваться при расчетах, связанных с извлечением этана и пропана при низких температурах. Параметрами графиков, составленных Прайсом, являются давление, температура и фазовые средние мольные точки кипения [XV. 266]. Некоторые экспериментально полученные данные для системы метан — этан — пропан приведены в табл. XV. 2, а константы равновесия для системы метан — пропан даны на рис. XV. 13.
Курата и его сотрудники, изучая фазовое поведение природных газов, составили фазовые диаграммы и определили критические точки при низких температурах [XV. 14, XV. 18]. Составы газов и их характеристика при критических условиях даны в табл. XV. 2. Фазовое поведение смеси А-4, состав которой приведен в табл. XV. 3, представлено на рис. XV. 14 и XV. 15 Кривая коэффициента сжимаемости была построена на основании имеющихся экспериментальных данных о давлении, объеме и температуре газов вплоть до интервала иизких температур (рис. XV. 16). В некоторых случаях в смеси находились две фазы.
0.002
0,ООП 0,00k от 0,02 0,0h 0,0Ь 0,1 02 0,^ 06081
2 Ч 6 8 10 20 ЬО 6060Ю0
Щ6
Абсолютное давление) ат
Рис. XV. 13. Консъанты , равновесия для системы метан — пропан [XV. 26а].
/ — по Прайсу; 2— по Сейджей. Лейси; 3— по Акерсу, Бернсу и Фейрчайлду; 4—упругость паров; 5 — закон* Генри; 6 — метан; 7 — пропан.
Абсолютное давление, ат
|
Состав жидкой фазы |
Состав | газообразн | ой фазы |
Константы равновесия К | ||||
| СН, |
С2На |
С3Н„ |
СН4 |
с2н„ |
с3н. | СН, |
сгн. | СзН„ |
| 0,0028* |
0,998 | 0,057 | 0,943 | 20,5* |
0,945 | |||
|
0,0022* | .0,0080 |
0,9897 | 0,0452 |
0,0280 | 0,9268 |
20,4* | 3,50 |
0^936 |
|
0,0236 | 0,9764 |
•— | 0,0720 |
0,9280 | — |
3,05 | 0,951 | |
| 0,044* | .— |
0,960 | 0,471 | 0,529 | 10,7* |
0,551 | ||
|
0,044* | — |
0,962 | 0,471 |
__ | 0,529 |
10,7* | 0,550 |
|
| 0,0396* | 0,0655 | 0,8966 | 0,412 | 0,112 | 0,476 |
10,4* | 1,86 |
0*531 |
| 0,0270* |
0,160 | 0,811 |
0,275 | 0,284 |
0,441 | 10,1* |
1,78 | 0,545 |
| 0,0128* | 0,264 |
0,7193 | 0,127 |
0,476 | 0,397 |
9,95 | 1,80 |
0,552 |
|
0,357 | 0,643 |
•— | 0,612 |
0,388 | — |
1,72 | 0,603 | |
| 0,128 | _ |
0,872 | 0,685 |
__ | 0,315 |
5,35 | 0,361 |
|
| 0,110 | 0,175 |
0,715 | 0,557 |
0,193 | 0,250 |
5,06 | 1,10 |
0,350 |
| 0,0697 |
0,500 | 0,4303 |
0,306 | 0,535 |
0,159 | 4,39 |
1,07 | 0,369 |
| 0,0620 | 0,553 |
0,385 | 0,282 |
0,570 | 0,148 |
4,54 | 1,03 |
0.348 |
| 0,0302 |
0,7578 | 0,212 |
0,115 | 0,7989 |
0,0861 | 3,81 |
1.05 | 0,406 |
| — | 0,9066 |
0,0934 | — |
0,9616 | 0,0384 |
1,06 | 1,06 |
0,411 |
| ' |
0,9108 | 0,0892 |
— | 0,9606 |
0,0394 | — |
1,05 | 0,442 |
| 0,216 | _ |
0,784 | 0,762 | 0,238 | 3,53 |
0,304 | ||
|
0,214 | 0,151 |
0,635 | 0,663 |
0,133 | 0,204 |
3,10 | 0,880 |
0,321 |
| 0,204 |
0,178 | 0,618 |
0,654 | 0,150 |
0,196 | 3,20 |
0,843 | 0,317 |
| 0,178 | 0,376 |
0,446 | 0,521 |
0,332 | 0,147 |
2,93 | 0,883 |
0,330 |
| 0,174 |
0,457 | 0,369 |
0,487 | 0,382 |
0,131 | 2,80 |
0,836 | 0,355 |
| 0,137 | 0,647 |
0216 | 0,371 |
0,5501 | 0,0789 |
2,71 | 0,849 |
0,365 |
| 0,113 |
0,768 | 0,119 |
0,286 | 0,6668 |
0,0472 | 2,53 |
0,868 | 0,397 |
|
0,083 | 0,917 |
— | 0,210 |
0,790 | — |
2,53 | 0,861 | |
| 0,300 | _. |
0,700 | 0,788 |
; _ | 0,212 |
2,63 | 0,303 |
|
| 0,286 | 0,121 |
0,593 | 0,7224 |
i 0,9606 | 0,187 |
2,53 | 0,749 |
0,315 |
| 0,268 |
0,359 | 0,373 |
0,588 | : 0,282 |
0,130 | 2,19 |
0,786 | 0,348 |
| 0,255 | 0,454 |
0,291 | 0,534 |
0,357 | 0,109 |
2,10 | 0,787 |
0,374 |
| 0,237 |
0,566 | 0,197 |
0,4632 | 0,455 |
0,0818 | 1,95 |
0,803 | 0,415 |
| 0,207 | 0,793 |
— | 0,325 |
0,675 | — |
1,58. | 0,852 | |
| 0,413 | _ |
0,587 | 0,805 |
_ | 0,195 |
1,95 | 0,332 |
|
| 0,389 | 0,169 | 0,442 | 0,707 |
0,126 | 0,167 |
1,82 | 0,745 |
0,378 |
| 0,385 |
0,225 | 0,390 |
0,680 | 0,164 |
0,156 | 1,76 |
0,729 | 0,400 |
| 0,373 | 0,357 |
0,270 | 0,600 |
0,268 | 0,132 |
1,61 | 0,751 |
0,442 |
| 0,349 |
0,505 | 0,146 |
0,4826 | 0,431 |
0,0864 | 1,38 |
0,853 | 0,591 |
| 0,3755 | 0,5241 |
0,1004 | 0,4345 |
0,490 | 0,0755 |
1,16 | 0,933 |
0,751 |
| 0,451 |
_ | 0,549 |
0,803 | 0,197 |
1,78 | 0,359 | ||
| 0,4365 |
0,0409 | 0,5226 |
0,7746 | 0,0306 |
0,1948 | 1,77 |
0,748 | 0,373 |
| 0,430 | 0,110 |
0,460 | 0,7341 |
0,0849 | 0,181 |
1,71 | 0,771 |
0,394 |
| 0,438 |
0,192 | 0,370 |
0,692 | 0,143 |
0,165 | 1,58 |
0,744 | 0,446 |
| 0,438 | 0,223 |
0,339 | 0,665 |
0,173 | 0,162 |
1,52 | 0,776 |
0,478 |
| 0,435 |
0,259 | 0,306 |
0,630 | 0,209 |
0,161 | 1,45 |
0,807 | 0,526 |
| 0,440 | 0,376 |
0,184 | 0,504 |
0,351 | 0,145 |
1,15 | 0,394 |
0,778 |
| 0,498 |
_ | 0,502 |
0,784 | 0,216 |
1,57 | 0,430 | ||
| 0,4997 |
0,0375 | 0,4628 |
0,7558 | 0,0302 |
0,214 | 1,51 |
0,806 | 0,462 |
| 0,504 | 0,176 |
0,320 | 0,673 |
0,143 | 0,184 |
1,34 | 0,813 |
0,575 |
| 0,508 |
0,243 | 0,249 |
0,584 . | 0,219 |
0,197 | 1,15 |
0,901 | 0,791 |
№
по
коду
Температура, °С
| 1 |
10,0 | 7 |
|
2 | 10,0 | 7 |
| 3 | 10,0 |
7 |
| 5 |
10,0 | 14 |
|
6 | 10,0 | 14 |
| 7 | 10,0 |
14 |
| 8 |
10,0 | 14 |
|
9 | 10,0 | 14 |
| 10 | 10,0 |
14 |
| 11 |
10,0 | 28 |
|
12 | 10,0 | 28 |
| 13 | 10,0 |
28 |
| 14 |
10,0 | 28 |
|
15 | 10,0 |
28 |
| 16 |
10,0 | 28 |
|
17 | 10,0 | 28 |
| 18 | 10,0 | 42 |
| 19 | 10,0 | 42 |
| 20 | 10,0 |
42 |
| 21 |
10,0 | 42 |
|
22 | 10,0 | 42 |
| 23 | 10,0 |
42 |
| 24 |
10,0 | 42 |
|
25 | 10,0 |
42** |
| 26 |
10,0 | 56 |
|
27 | 10,0 | 56 |
| 28 | 10,0 | 56 |
| 29 | 10,0 | 56 |
| 30 | 10,0 |
56 |
| 31 |
10,0 | 56** |
|
32 | 10,0 | 70 |
| 33 | 10,0 | 70 |
| 34 | 10,0 | 70 |
| 35 | 10,0 |
70 |
| 36 |
10,0 | 70 |
|
37 | 10,0 | 70 |
| 38 | 10,0 | 77 |
| 39 | 10,0 | 77 |
| 40 | 10,0 |
77 |
| 41 |
10,0 | 77 |
|
42 | 10,0 | 77 |
| 43 | 10,0 | 77 |
| 44 | 10,0 | 77 |
| 45 | 10,0 |
84 |
| 46 |
10,0 | 84 |
|
47 | 10,0 | 84 |
| 48 | 10,0 | 84 |
|
№ по коду |
Температура, °С |
Абсолютное давление, ат | Состав жидкой фазы |
Состав | газообразной фазы | Константы равновесия К | |||||
|
СН4 | С2н„ |
С3н, | СН4 |
с„н„ |
с3п, | СН4 |
С2На | С,н, | |||
| 49 |
—17,8 | 7 |
0,3538 | 0,9642 |
0,573 | 0,427 | 15,9 |
0,445 | |||
| 50 |
— 17,8 | 7 |
0,3335 | 0,0174 |
0,9491 | 0,5589 |
0,0336 | 0,4075 |
16,7 | 1,93 |
0,430 |
| 51 |
—17,8 | 7 |
0,0279 | 0,1284 |
0,8437 | 0,400 |
0,246 | 0,354 |
14,3 | 1,92 |
0,420 |
| 52 |
— 17,8 | 7 |
0,0210 | 0,166 |
0,813 | 0,325 |
0,349 | 0,326 |
15,5 | 2,10 |
0,401 |
| 53 |
— 17,8 | 7 |
0,0107 | 0,272 |
0,7173 | 0,159 |
0,534 | 0,307 |
14,9 | 1,96 |
0,428 |
| 54 |
— 17,8 | 7 |
— | 0,373 |
0,627 | — |
0,692 | 0,308 |
— | 1,85 |
0,491 |
| 55 |
— 17,8 | 14 |
0,0904 | 0,9096 |
0,768 | _ |
0,232*** | 8,47 |
.— | 0,256 | |
| 56 | — 17,8 |
14 | 0,0917 |
0,0127 | 0,8596 |
0,7717 | 0,0133 |
0,215 | 8,43 |
1,05 | 0,240 |
| 57 | — 17,8 |
14 | 0,0702 |
0,250 | 0,6798 |
0,560 | 0,270 |
0,170 | 7,98 |
1,08 | 0,250 |
| 58 | — 17,8 |
14 | 0,0457 |
0,4843 | 0,470 |
0,359 | 0,519 |
0,122 | 7,85 |
1,07 | 0,260 |
| 59 | — 17,8 |
14 | 0,0127 |
0,8133 | 0,174 |
0,0778 | 0,8746 |
0,0476 | 6,12 |
1,08 | 0,274 |
| 60 | — 17,8 |
14 | — |
0,9013 | 0,0987 |
— | 0,9717 |
0,0283 | — |
1,08 | 0,287 |
| 61 | — 17,8 |
28 | 0,199 |
0,801 | 0,862 |
_ | 0,138 |
4,33 | _ |
0,172 | |
| 62 |
— 17,8 | 28 |
0,159 | 0,347 |
0,494 | 0,6985 |
0,127 | 0,0845 |
4,39 | 0,626 |
0,171 |
| 63 |
— 17,8 | 28 |
0,1557 | 0,5293 |
0,315 | 0,6003 |
0,343 | 0,0567 |
3,86 | 0,648 |
0,180 |
| 64 |
— 17,8 | 28 |
0,1364 | 0,7243 |
0,1393 | 0,4869 |
0,4852 | 0,0279 |
3,57 | 0,670 |
0,200 |
| 65 |
— 17,8 | 28** |
0,123 | 0,877 |
— | 0,410 |
0,590 | — |
3,33 | 0,673 | |
| 66 | — 17,8 |
42 | 0,311 | 0,689 | 0,891 |
_ | 0,109 |
2,86 | _ |
0,158 | |
| 67 |
— 17,8 | 42 |
0,293 | 0,266 |
0,441 | 0,781 |
0,1377 | 0,0813 |
2,67 | 0,518 |
0,185 |
| 68 |
— 17,8 | 42 |
0,288 | 0,343 |
0,369 | 0,7514 |
0,184 | 0,0646 |
2,61 | 0,537 |
0,175 |
| 69 |
—17,8 | 42 |
0,272 | 0,481 |
0,247 | 0,6896 |
0,260 | 0,0504 |
2,54 | 0,540 |
0,204 |
| 70 |
—17,8 | 42 |
0,271 | 0,6204 |
0,1086 | 0,6138 |
0,361 | 0,0252 |
2,28 | 0,582 |
0,232 |
| 71 |
—17,8 | 42** |
0,256 | 0,744 |
- | 0,561 |
0,439 | — |
2,18 | 0,591 | |
| 72 | — 17,8 | 56 | 0,415 |
0,585 | 0,899 | _ | 0,101 |
2,16 | _ |
0,173 | |
| 73 |
— 17,8 | 56 |
0,391 | 0,188 |
0,421 | 0,8239 |
0,0339 | 0,0822 |
2,11 | 0,499 |
0,196 |
| 74 |
— 17,8 | 56 |
0,378 | 0,354 |
0,268 | 0,7727 |
0,1702 | 0,0517 |
2,05 | 0,481 |
0,213 |
| 75 |
— 17,8 | 56 |
0,380 | 0,418 |
0,202 | 0,7318 |
0,224 | 0,0442 |
1,93 | 0,536 |
0,219 |
| 76 |
— 17,8 | 56 |
0 380 | 0,5142 |
0,1058 | 0,6795 |
0,296 | 0,0245 |
1,80 | 0,576 |
0,232 |
| 77 |
—17,8 | 56** |
0,390 | 0,610 |
— | 0,619 |
0,381 | — |
1,59 | 0,621 | |
| 78 | —17,8 | 70 | 0,522 |
0,278 | 0,895 | _ | 0,105 |
1,71 | _ | 0,220 | |
| 79 |
—17,8 | 70 |
0,515 | 0,0780 |
0,407 | 0,8623 |
0,0443 | 0,0934 |
1,63 | 0,568 |
0,230 |
| 80 |
— 17,8 | 70 |
0,512 | 0,187 |
0,301 | 0,8174 |
0,1027 | 0,0799 |
1,60 | 0,549 |
0,266 |
| 81 |
— 17,8 | 70 |
0,514 | 0,239 |
0,247 | 0,791 |
0,140 | 0,0690 |
1,54 | 0,586 |
0,280 |
| 82 |
— 17,8 | 70 |
' 0,5161 | 0,3378 |
0,1461 | 0,7234 |
0,226 | 0,0506 |
1,40 | 0,669 |
0,346 |
| 83 . |
— 17,8 | 70 |
0,5258 | 0,4467 |
0,0275 | 0,6357 |
0,349 | 0,0153 |
1,21 | 0,781 |
0,554 |
| 84 |
— 17,8 | 70** |
, 0,522 | 0,478 |
— | 0,569 |
0,431 | — |
1,09 | 0,901 | |
| 85 | — 17,8 | 77 | 0,582 |
0,418 | 0,888 |
0,112 | 1,53 |
_ | 0,268 | ||
|
86 | — 17,8 |
77 | 0,5759 |
0,0581 | 0,366 |
0,8619 | 0,0341 |
0,104 | 1,50 |
0,587 | 0,284 |
| 87 | — 17,8 |
77 | 0,585 |
0,107 | 0,308 |
0,8377 | 0,0635 |
0,0988 | 1,43 |
0,593 | 0,321 |
| 88 | — 17,8 |
77 | 0,584 |
0,157 | 0,259 |
0,8237 | 0,0928 |
0,0835 | 1,41 |
0,591 | 0,322 |
| 89 | — 17,8 |
77 | 0,578 |
0,192 | 0,221 |
0,7947 | 0,1231 |
0,0822 | 1,35 |
0,641 | ¦ 0,372 |
| 90 | — 17,8 |
77 | 0,582 |
0,228 | 0,190 |
0,7707 | 0,154 |
0,0753 | 1,32 |
0,675 | : 0,396 |
| 91 | — 17,8 | 77 |
0,5917 | 0,2483 |
0,1600 | 0,7945 |
0,1758 | 0,0697 |
1,275 | 0,708 |
г' 0,436 |
|
92 | —17,8 |
77 | 0,6043 |
0,259 | 0,1367 |
0,7484 | 0,1855 |
0,0661 | 1,24 |
0,716 | i 0,484 |
| 93 | —17,8 |
77 | 0,604 |
0,273 | 0,123 |
¦0,7142 | 0,2177 |
0,0681 | 1,18 | ¦ 0,797 | . 0,554 |
| 94 | —17,8 |
84 | 0,637 |
0,363 | 0,873 | 0,127 | 1,37 |
_ | 0,350 | ||
|
95 | —17,8 |
84 | 0,6456 | , 0,0874 | 0,267 |
0,8218 | 0,0625 |
0,1157 | 1,27 |
i 0,716 | 0,433 |
| 96 | —17,8 |
84 | 0,653 |
¦0,106 | 0,241 |
0,8158 | 0,0751 |
¦0,1091 | 1,25 |
„ 0,708 | 0,453 |
| 97 | —17,8 |
84 | 0,650 |
0,118 | 0,232 |
0,795 | 0,089 |
0,116 | 1,22 |
0,754 | 0,500 |
| 98 | — 17,8 |
84 | 0,693 |
0,161 | 0,146 |
0,721 | 0,144 |
.0,135 | 1,04 |
0,894 | i 0,925 |
|
№ по ходу |
Температура, °С |
Абсолютное давление, ат 1 |
Состав жидкой |
фазы | Состав газообразной фазы |
Константы равновесия К | |||||
|
СН„ | с2Н„ |
С3Н„ | СН4 |
С2Н„ | СЭН„ | СН | С2Н„ |
СдН о | |||
| 99 |
— 17,8 | 91 |
0,708 | 0,292 |
0,845 | 0,155 | 1,19 |
0,531 | |||
| 100 |
— 17,8 | 91 |
0,7103 | 0,0297 |
0,260 | 0,8294 |
0,0246 | 0,146 |
1,17 | 0,828 |
0,561 |
| 101 |
— 17,8 | 91 |
0,7315 | 0,0345 |
0,234 | 0,8086 |
0,0322 | 0,1592 |
1,11 | 0,933 |
0,681 |
| 102 |
— 17,8 | 91 |
0,7364 | 0,0396 |
0,224 | 0,7978 |
0,0384 | 0,1638 |
1,08 | 0,970 |
0,731 |
| 103 |
—45,6 | 7 |
0,0769 | 0,9231 |
0,840 | _ |
0,160 | 10,9 |
_ | 0,173 | |
|
104 | —45,6 |
7 | 0,0614 |
0,1718 | 0,7668 |
0,7195 | 0,1628 |
0,1177 | 11,7 |
0,947 | 0,153 |
| 105 | —45,6 |
7 | 0,0486 |
0,302 | 0,6494 |
0,605 | 0,292 |
0,103 | 12,4 |
0,967 | 0,159 |
| 106 | —45,6 |
7 | 0,0479 |
0,399 | 0,5531 |
0,5287 | 0,380 |
0,0913 | 11,00 |
0,952 | 0,165 |
| 107 | —45,6 |
7 | 0,0467 |
0,448 | 0,5053 |
0,4952 | 0,425 |
0,0798 | 10,6 |
0,949 | 0,158 |
| 108 | —45,6 |
7 | 0,0261 |
0,7259 | 0,248 |
0,280 | 0,682 |
0,0380 | 10,7 |
0,938 | 0,153 |
| 109 | —45,6 |
0,006 | 0,994 | — | 0,066 |
0,934 | — | 11,0 | 0,940 | ||
|
110 | —45.6 |
14 | 0,146 |
0,854 | 0,9216 |
_ | 0,0784 |
6,31 | _ |
0,0918 | |
| 111 |
—45,6 | 14 |
0,125 | 0,268 |
0,607 | 0,804 |
0,140 | 0,0560 |
6,43 | 0,522 |
0,0922 |
| 112 |
—45,6 | 14 |
0,125 | 0,368 |
0,507 | 0,7478 |
0,206 | 0,0462 |
5,98 | 0,560 |
0,0911 |
| 113 |
—45,6 | 14 |
0,119 | 0,627 |
0,254 | 0,6383 |
0,333 | 0,0287 |
5,35 | 0,531 |
0,115 |
| 114 |
—45,6 | 14 |
0,9032 | — |
0,505 | 0,505 |
0,495 | — |
5,22 | 0,548 | |
| 115 | —45,6 | 28 | 0,296 |
0,704 | 0,9493 | _ | 0,0507 |
3,20 | _ |
0,0735 | |
| 116 |
—45,6 | 28 |
0,292 | 0,126 |
0,582 | 0,920 |
0,0383 | 0,0417 |
3,15 | 0,304 |
0,0717 |
| 117 |
—45,6 | 28 |
0,271 | 0,289 |
0,440 | 0,8791 |
0,0907 | 0,0302 |
3,24 | 0,314 |
0,0687 |
| 118 |
—45,6 | 28 |
0,274 | 0,448 |
0,278 | 0,8245 |
0,154 | 0,0215 |
3,02 | 0,344 | 0 0773 |
| 119 |
—45,6 | 28 |
0,270 . | 0,512 |
0,218 | 0,8084 |
0,1742 | 0,0171 |
2,99 | 0,340 |
0,0798 |
| 120 |
—45,6 | 28 |
0,277 | 0,523 |
0,200 | 0,7986 |
0,1880 | 0,0134 |
2,88 | 0,359 |
0,0805 |
| 121 |
—45,6 | 28 |
0,278 | 0,571 |
0,151 | 0,7901 |
0,194 | 0,0159 |
2,74 | 0,340 |
0,105 |
| 122 |
—45,6 | 28 |
0,282 | 0,718 |
— | 0,724 |
0,276 | — |
2,57 | 0,384 | |
| 123 | —45,6 | ,42 | 0,438 |
0,562 | 0,9585 | _ | 0,0415 |
2,19 | _ |
0,0739 | |
| 124 |
—45,6 | 42 |
0,440 | 0,145 |
0,415 | 0,9179 |
0,0485 | 0,0336 |
2,06 | 0,334 |
0,0809 |
| 125 |
—45,6 | 42 |
0.424 | 0,150 |
0,426 | 0,919 |
0,0446 | 0,0364 |
2,17 | 0,298 |
0,0855 |
| 126 |
—45,6 | 42 |
0,443 | 0,243 |
0,314 | 0,8952 |
0,0790 | 0,0258 |
2,02 | 0,325 |
0,0822 |
| 127 |
—45,6 | 42 |
0,441 | 0,366 |
0,193 | 0,8637 |
0,119 | 0,173 |
1,96 | 0,327 |
0,0896 |
| 128 |
—45,6 | 42 |
0,438 | 0,562 |
— | 0,800 | 0,200 | — | 1,83 |
0,356 | |
| 129 | —45,6 | 56 |
0,581 | 0,419 | 0,959 | _ |
0,0410 | 1,65 |
_ | 0,0978 | |
|
130 | —45,6 |
56 | 0,598 |
0,109 | 0,293 |
0,9275 | 0,362 |
0,0363 | 1,55 |
0,332 | 0,124 |
| 131 | —45,6 |
56 | 0,611 |
0,249 | 0,140 |
0,8901 | 0,0886 |
0,0213 | 1,46 |
0,356 | 0,152 |
| 132 | —45,6 |
56 | 0,622 |
0,378 | — |
0,832 | 0,168 |
— | 1,34 |
0,445 | |
| 133 | —45,6 | 70 |
0,736 | 0,264 | 0,9458 |
0,0542 | 1,29 |
_ | 0,205 | ||
|
134 | —45,6 |
70 | 0,7609 |
0,0651 | 0,174 |
0,9216 | 0,0331 |
0,0453 | 1,21 |
0,509 | 0,260 |
| 135 | —45,6 |
70 | 0,7662 |
0,0892 | 0,1446 |
0,9026 | 0,0504 |
0,0470 | 1,18 |
0,565 | 0,325 |
| 136 | —45,6 |
70 | 0,7749 |
0,1261 | 0,0990 |
0,8838 | 0,0758 |
0,0404 | 1,14 |
0,609 | 0,408 |
| 137 | —45,6 |
70 | 0,7837 |
0,1491 | 0,0672 |
0,8631 | 0,1001 |
0,0368 | 1,10 |
0,671 | 0,547 |
| 138 | —45,6 |
70 | 0,8332 |
0,1318 | 0,0350 |
0,8363 | 0,1288 |
0,0349 | 1,00 |
0,977 | 0,997 |
| 139 | —73,3 |
7 | 0,125 |
0,875 | 0,9591 | 0,0409 | 7,67 |
_ | 0,0468 | ||
|
140 | —73,3 |
7 | 0,118 |
0,144 | 0,738 |
0,9186 | 0,0472 |
0,0342 | 7,78 |
0,328 | 0,0463 |
| 141 | —73,3 |
7 | 0,110 |
0,320 | 0,570 |
0,8651 | 0,110 |
0,0249 | 7,77 |
0,344 | 0,0437 |
| 142 | —73,3 |
7 | 0,110 |
0,580 | 0,310 |
0,7916 | 0,194 |
0,0144 | 7,20 |
0,334 | 0,0464 |
| 143 | —73,3 |
7 | 0,101 |
0,899 | — |
0,680 | 0,320 |
— | 6,73 |
0,356 | |
| 144 | —73,3 | 14 |
0,222 | 0,778 |
0,9792 | 0,0208 | 4,41 | _ |
0,0268 | ||
| 145 |
—73,3 | 14 |
0,235 | 0,121 |
0,644 | 0,9615 |
0,228 | 0,0157 |
4,09 | 0,188 |
0,0254 |
| 146 |
—73,3 | 14 |
0,232 | 0,435 |
0,333 | 0,9070 |
0,0840 | 0,00897 |
3,91 | 0,193 |
0,0269 |
| 147 |
—73,3 | 14 |
0,236 | 0,483 |
0,281 | 0,8926 |
0,0983 | 0,00909 |
3,78 | 0,204 |
0,0324 |
| 148 |
—73,3 | 14 |
0,250 | 0,750 |
—¦ | 0,814 |
0,186 | —¦ |
3,26 | 0,248 | |
|
№ по коду | Температура. *С | Абсолютное давление, ат | Состав жидкой фазы | Состав газообразной фазы | Константы равновесия К | ||||||
| сн4 |
С2н, |
С3Н8 | СН4 | С2Нв |
С3Н, | СН, |
С2Н, | С3Н„ |
|||
| 149 | —73,3 |
28 | 0,477 |
0,523 | 0,9855 |
0,0145*** | 2,06 |
0,0277 | |||
| 150 |
—73,3 | 28 | 0,492 |
0,175 | 0,333 | 0,963 | 0,0266 | 0,0104 |
1,96 | 0,152 | 0,0312 |
| 151 | —73,3 |
28 | 0,496 | 0,242 |
0,262 | 0,9562 |
0,0364 | 0,00741 | 1,93 | 0,150 | 0,0283 |
| 152 | —73,3 | 28 | 0,504 | 0,308 |
0,188 | 0,9446 | 0,0486 | 0,00685 | 1,88 |
0,168 | 0,0364 |
|
153 | —73,3 | 28 |
0,5191 | 0,386 |
0,0949 | 0,9321 | 0,0630 | 0,00486 | 1,80 |
0,163 | 0,0512 |
|
154 | —73,3 | 28 |
0,528 | 0,472 | — | 0,9165 | 0,0835 |
— | 1,72 | 0,177 |
|
| 155 | —73,3 | 42 | 0,744 | _ | 0,256 | 0,9852 | 0,0148 | 1,32 |
0,0556 | ||
| 156 |
—73,3 | 42 | 0,745 |
0,0520 | 0,203 |
0,9775 | 0,0119 | 0,0106 | 1,31 | 0,229 |
0,0522 |
| 157 |
—73,3 | 42 | 0,7647 |
0,1612 | 0,0741 |
0,9583 | 0,0366 | 0,00512 | 1,25 | 0,227 |
0,0691 |
| 158 |
—73,3 | 42 | 0,784 |
0,216 | — | 0,9498 | 0,0502 | — |
1,21 | 0,232 | |
| 159 | —101,1 | 7 | 0,238 | _ |
0,762 | 0,9932 |
0,0068 | 4,17 |
0,0089 | ||
| 160 | — 101,1 | 7 | 0,242 |
0,258 | 0,500 | 0,9686 | 0,0282 | 0,0032 |
4,00 | 0,109 | 0,0064 |
| 161 | — 101,1 |
7 | 0,240 | 0,275 | 0,485 | 0,9653 |
0,0308 | 0.0039 | 4,02 | 0,112 | 0,9080 |
| 162 | — 101,1 | 7 | 0,249 | 0,446 |
0,305 | 0,9538 | 0,0433 | 0,0030 | 3,68 |
0,0970 | 0,0098 |
|
163 | — 101,1 | 7 |
0,252 | 0,6762 |
0,0718 | 0,9299 | 0,0682 | 0,0019 | 3,67 |
0,102 | 0,0265 |
|
164 | — 101,1 | 7 |
0,251 | 0,749 | — | 0,9312 | 0,0688 |
— | 3,71 | 0,0918 |
|
| 165 | — 101,1 | 14 | 0,502 | _ | 0,498 | 0,9955 | 0,0045 | 1,98 |
0,0090 | ||
| 167 | — 101,1 | 14 | 0,514 |
0,208 | 0,278 | 0,9806 | 0,0167 | 0,0027 |
1,91 | 0,0805 | 0,0097 |
| 168 | — 101,1 |
14 | 0,528 | 0,319 | 0,153 | 0,9742 |
0,0234 | 0,0024 | 1,84 | 0,0734 | 0,0157 |
| 169 | — 101,1 | 14 | 0,5532 | 0,400 |
0,0468 | 0,969 | 0,0294 | 0,0016 | 1,75 |
0,0735 | 0,0342 |
|
170 | — 101,1 | 14 |
0,561 | 0,439 | — | 0,970 | 0,030 |
— | 1,73 | 0,0683 |
|
| 171 | —128,8 | 7 | 0,802 | _ | 0,198 | 0,9993 | 0,0007 | 1,24 |
0,0035 | ||
| 172 | — 128,8 | 7 | 0,8075 |
0,0735 | 0,119 |
0,9962 | 0,0021 | 0,0007**** | 1,23 | 0,0286 |
0,0059 |
| 173 | — 128,8 | 7 | 0,8187 |
0,124 | 0,0573 |
0,9961 | 0,0029 | 0,0007**** | 1,22 | 0,0234 |
0,012 |
| 175 | — 128,8 | 7 | 0,833 |
0,167 | — | 0,9965 | 0,0035 | — |
1,20 | 0,0210 | |
* Вычислено по закону Генри. ** Блумер. *** Интерполяция. **** Расчет.
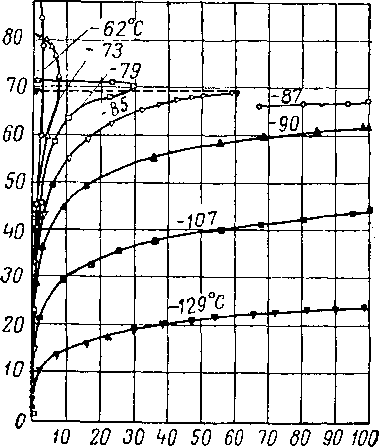
Рис. XV. 14. Изотермы смеси А—4 [XV. 14].
%
5
¦§
?
Ч:
Содержание жидкости °fa off
|
Газовая смесь | А-1 | А-2 | А-3 |
А-4 | АВ-1 | АВ-2 | АВ-3 | в |
С | D |
|
Молярная концентрация | 1,00 |
0,91 | ||||||||
| Двуокись углерода.......... | 1,20 |
1,09 | 0,44 |
0,30 | 0,20 |
0,13 | 0,20 |
0,25 | ||
| — |
— | — | — | —. | — |
— | 1,00 | 0,60 | 0,31 | |
|
— | 8,84 |
16,11 | 21,41 |
— | 11,30 |
24,00 | 11,46 |
13,50 | 7,05 | |
| 90,89 | 82,86 | 76,25 | 68,70 |
96,68 | 85,80 |
73,64 | 76,65 |
71,15 | 85,32 | |
| 4,40 | 4,01 | 3,69 | 3,33 |
1,60 | 1,50 |
1,20 | 5,51 | 6,10 | 4,11 | |
|
1,91 | 1,74 |
1,60 | 1,44 |
0,70 | 0,60 |
0,53 | 3,35 |
3,27 | 1,98 | |
| 0,33 |
0,30 | 0,28 |
0,30 | 0,14 |
0,12 | 0,10 | 0,35 | 0,38 | 0,37 |
|
| 0,60 | 0,55 | 0,51 | 0,40 |
0,20 | 0,18 |
0,15 | 0,90 |
0,60 | 0,39 | |
| Изопеитаи.............¦ |
0,21 | 0,19 | 0,18 | 0,16 | 0,07 |
0,06 | 0,05 |
0,17 | ||
| 0,13 | 0,12 |
0,11 | 0,10 | 0,05 | 0,04 | 0,04 |
0,15 | 0,20 |
0,22 | |
|
Гексаны............... | 0,15 | 0,14 | 0,12 |
0,11 | 0,05 |
0,04 | 0,04 | |||
| Гептаны и более тяжелые углеводороды . |
0,18 | 0,16 |
0,15 | 0,14 |
0,07 | 0,06 |
0,05 | 0,33 |
77,49 | 64,26 |
| Критическое абсолютное давление, ат . |
64,75 | 66,85 |
67,76 | 68,11 |
53,55 | 55,30 |
57,05 | 80,01 | ||
| Критическая температура, °К..... Критическая плотность, г/моль .... | 211,5 0,230 |
204 0,242 |
197,6 0,279 | 189 0,311 | 199,5 0,183 | 190,5 0,220 |
182,5 0,225 | 209 0,266 | 205,5 0,270 | 202 0,27( |
|
Молярное среднее критическое давление, ат................. | 47,32 | 46,13 | 45,22 |
44,17 | 47,18 |
44,10 | 45,08 | 45,08 | 46,06 |
|
| Мольная средняя критическая температура, °К.............. Весовая средняя критическая температура, °К ............... Молярный средний молекулярный вес . |
205 | 197,6 |
192 | 185,5 |
196 | 188,5 |
178,8 | 199 |
185,5 | 196,5 |
| 227,2 | 214,4 |
204 | 193,8 |
205,5 | 191 |
177,8 | 222 | 211 | 210,2 | |
| 18,40 | 19,25 | 19,94 |
20,75 | 16,90 |
18,11 | 19,56 |
20,02 | 19,98 | 18,60 | |
| Весовой средний эквивалент молекулярного веса (W)............ | 22,26 |
21,47 | 20,80 |
20,22 | 18,54 |
18,00 | 17,62 |
22,85 | 21,25 |
20,19 |
| Молекулярная средняя температура кипения ,' °к .............. | 121,2 |
117,2 | 113,8 |
110,5 | 115 |
110,5 | 106 |
118,3 | 116,7 |
116 |
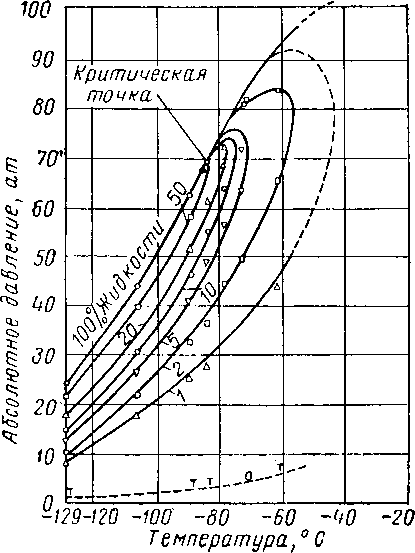
Рис. XV. 15, Фазовая диаграмма смеси А—4 [XV. 14].
О 0,2 ОА 0,6 0,8 1,11 иг 1,4 1,6 1,8
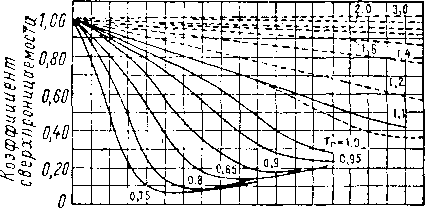
Рис. XV. 16. Коэффициенты Сверхсжимаемосги природных газов при низких температурах [XV. 14]:
Пунктирные кривые построены по Стендингу и Катцу.
Катц и его сотрудники изучали фазовое поведение систем, состоящих из водорода и легких углеводородов [XV. 3, XV. 5, XV. 6, XV. 36]. В этих системах при температурах до —185°С (точка замерзания углеводородов) водород обнаруживает обратную растворимость. Геометрическое место критических точек системы водород—метай показано иа рис. XV. 17, а константы равновесия этой системы — иа рис. XV. 18.
Этилен используется в качестве охлаждающего ве щества, поэтому знание его свойств необходимо для расчетов низкотемпературных процессов. Кривая зависимости энтальпии от давления для этилена, составленная Иорком и Уайтом [XV. 37], приведена иа рис. XV. 19.
Поскольку производственные процессы могут протекать при температуре или давлении, близких к критическим, представляют интерес критические свойства природных газов при низких температурах. Дэвис и другие [XV. 14] иа основе произведенных измерений
Рис. XV. 17. Диаграмма зависимости давления от температуры для системы водород — метай [XV. 5].
N
I
*
аГ
?
<У
300
/ — метан-, твердая фаза—жидкая фаза; 2 — геометрическое место критических точек; 3 — 40 %. в жидкой фазе: 4 — 20 % Н2 в жидкой фазе; 5 — 5 % Н2 в жидкой фазе; 6 — парь».
т
600,
|
т..... 1 /-1 1 1 | ||||||||
|
Теоретическое поведение | J Действительное поведение |
|||||||
| // * / '' | <•" | \К | 2 |
|||||
| /1 / ' | / / / / |
|||||||
| 130 | / ___ ? | 1 |
5 |
6 | ||||
| -260 _ 240 - 220 -200 ~П | W -It | '0 - wo |
||||||
Температура, °С
100
SO
40
20
10
8
4
Z
1,0
0,6
ОЛ
С»
«5>
«О
II
О?
«3
°’2 I 0,1 I 0,06
I 0,0 4
*0,02 о
е
| N |
V | |||||||
| V |
ч; | |||||||
| \ | \ | N |
v-:; | |||||
|
-V | \ \ | |||||||
| I | v \ | |||||||
|
.....ч |
% | о | i \ | |||||
| Ъ |
aSlL / |
~i / | ||||||
|
г / | ||||||||
|
\ | N | о с | 11 fT | |||||
| S |
'i'cP | -f--- J | ||||||
| > | / j |
f | ||||||
|
У |
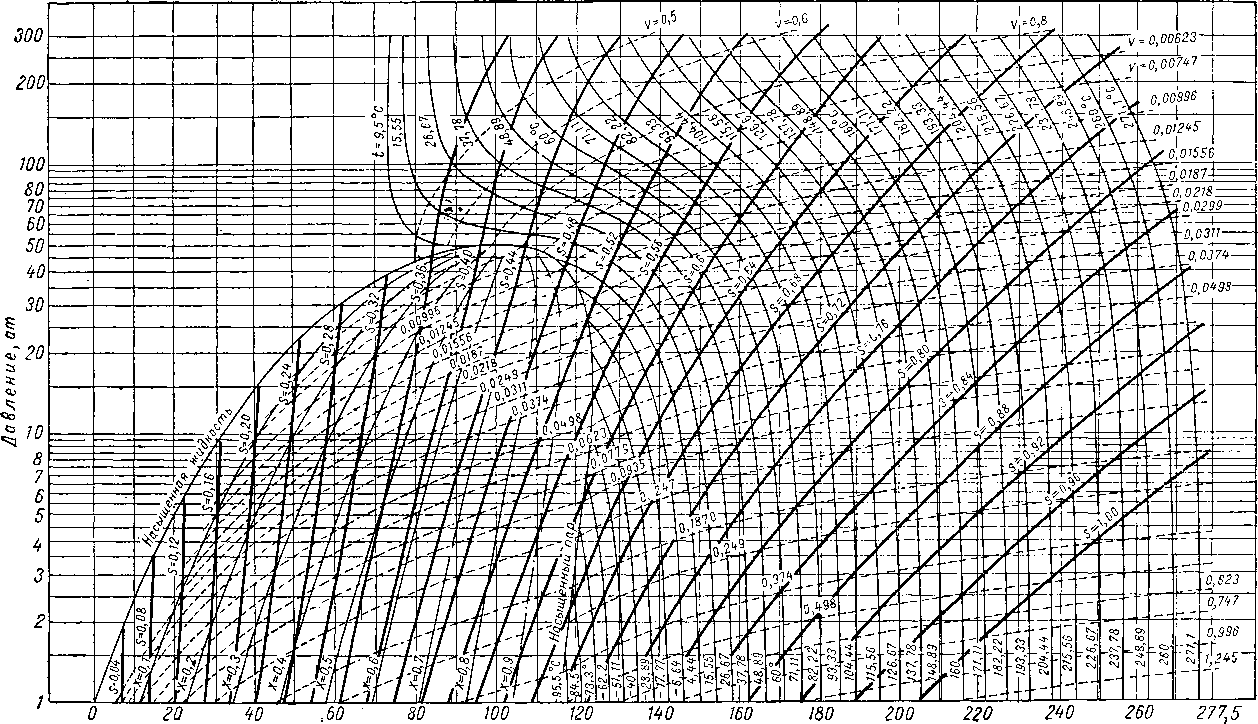
Энтальпия, ккал/ кг
Рис. XV. 19. Диаграмма, зависимости энтальпии от давления для этилена [XV. 37]. t—температура в °С; V ^ удельный объем в м* /кг\ S ~ удельная энтропия в ккал/кг СК; х'==. качество. Данные hj—О и ^ — 0 при —104° С и 1 ат.
ел
to
Рис. XV. 20. Уточненная диаграмма корреляции критического давления природных газов при низких температурах [XV. 14].

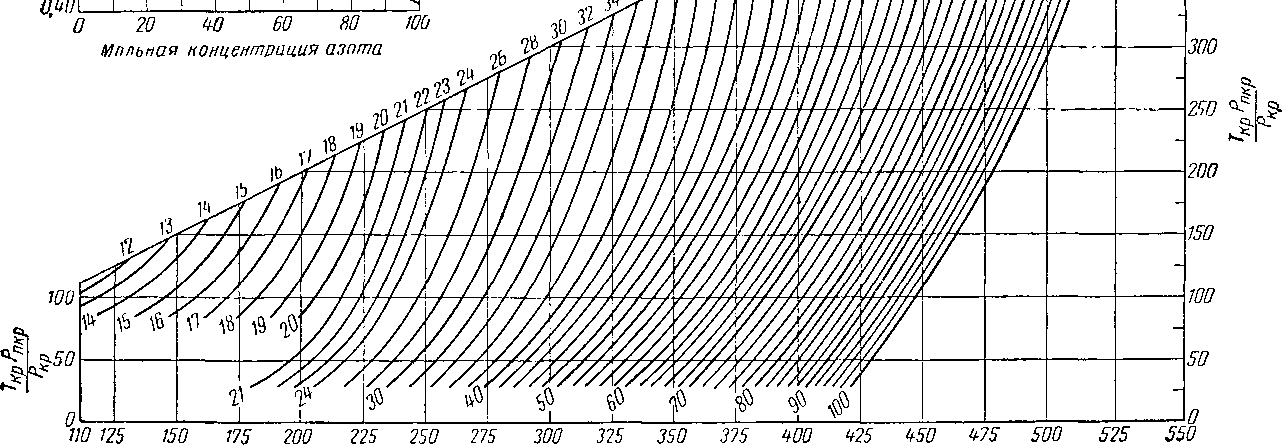
Г^- среднемольная критическая температура,0к
свойств природных газов при критических условиях пересмотрели график корреляции критических условий, составленный Курата и Катцем [IV. 52а]. Уточненный график приведен на рис. XV. 20. Критические температуры и давления определяют путем вычисления средневзвешенной критической температуры Тс с последующей корректировкой этой величины при помощи уравнения
Гс = Г'+ AU2m1m2 + AU3m1m3 + Л1>4т1т4 + . .. ,
(XV. 1)
где Тс — истинная критическая температура в °К; Тс — средневзвешенная критическая температура в °К; •/41.2—константа для системы 1,2 по табл. XV. 4; m — весовая доля; индексы 1,2... обозначают соответствующий компонент.
В уравнение (XV. 1) необходимо включить все возможные сочетания бинарных систем. Зная псевдокритические (средние мольные) величины давления рак и температуры Тпк, истинную критическую температуру и средний молекулярный вес М, можно по рис. XV. 20 оп-
Величины константы А для уравнения (XV.I) [XV. 14]
| Наиме нова ние |
N, | с, | Сг |
с, | С. | С, | с. | с, |
| Na | 0 | 0 | ||||||
| Cj | 20—53(N2) | 0 | ||||||
| С2 |
—83 | |||||||
| — 14 | —222 | 0 |
||||||
|
С3 | 0 | —17 | 0 | 0 | ||||
| с4 | —55 | —100 |
—15 | —6 | ||||
| с. |
—167 | —83 | —28 | —17 | 0 | 0 | ||
| Се |
—278 | —222 | —28 | —28 | 0 | — 14 | 0 | |
|
С, | —334 | —222 |
—55 | —28 | 0 | —55 | 0 | 0 |
| Сй |
—334 | —222 | —83 | —28 | —6 |
—55 | 0 | 0 |
|
—6 |
ределить истинное критическое давление для смеси рк-Если в смеси содержится азот, то для определения р„ по рис, XV. 20 берут величину М*. Гелий повышает критическое давление примерно на 7 кГ/см2 на каждый 1 % мол. содержания его в смеси.
§ 2. НИЗКОТЕМПЕРАТУРНАЯ ПЕРЕРАБОТКА ПРИРОДНОГО ГАЗА
Общее описание низкотемпературной переработки природного газа содержится в монографии Пратта и Фоскетта (Pratt and Foskett) [XV. 26]. Катц, Шатц и Уилльямс (Katz, Schatz and Williams) [XV. 20] рассмотрели равновесные условия для деэтанизационной низкотемпературной установки фирмы «Теннесси гэз транс-мишн компани» близ г. Гринсберг (штат Кентукки) [XV. 21]. Они показали, что интервал давления, при котором удаляются этан и более тяжелые углеводороды в установках однократного охлаждения, приближается к давлению схождения для системы на рис. XV. 21. Экспериментальные данные о сжижении природных газов, содержащих небольшое количество этана и более тяжелых углеводородов, представлены на рис. XV. 14. Для полного сжижения газа необходимо давление не более
10,5 ат при температуре —37,7° С.
Упомянутая установка фирмы «Теннесси гэз транс-мишн компани», построенная для извлечения этана и более тяжелых углеводородов, описана Кингом и Мертцем (King and Mertz) [XV. 17, XV. 21, XV. 23]. Пропускная способность установки по газу составляла первоначально 21,2 млн,м3/сутки, впоследствии она была повышена до 26,9 млн. м3/сутки, в результате чего выработка жидких углеводородов возросла до 1665 м3/сутки.
Принципиальная схема этой установки показана на рис. XV. 22.
Газ осушают до температуры точки росы —75,5° С при помощи активированной окиси алюминия. Для предотвращения образования гидратных пробок вводят метанол. Осушенный газ вступает в теплообмен сначала с остаточным газом, а затем с охладителем этана (при —71°С), где он отдает свою скрытую теплоту, и, наконец, с жидкостью, выходящей из испарителя. Первичную сепарацию производят при температуре —75,5° С и давлении 37,5 кГ/см2. Выход жидкости при этом составляет 5,5% мол. от потока. Остаточный газ после теплообмена компримируют и возвращают в газопровод. Смесь, используемую для охлаждения этана, конденсируют при температуре —20° С; конденсирующим агентом при этом служит пропан. Состав перерабатываемого и остаточного газа приведен в табл. XV. 5. Жидкие про-
-73,3° С
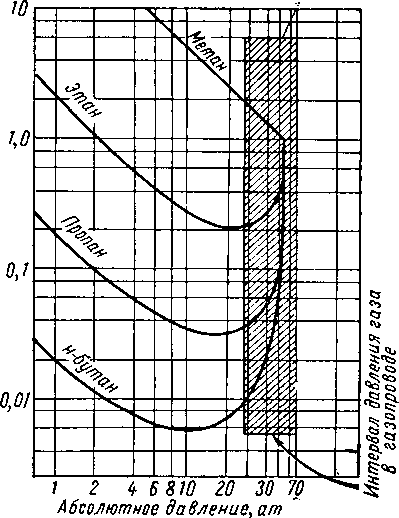
Рис. XV. 21. Константы равновесия для природных газов при температуре —73° С.
дукты подают на расположенный поблизости нефтехимический завод. Все конструктивные элементы, работающие в интервале температур ниже —29°С, изготовляются из никелевой стали.
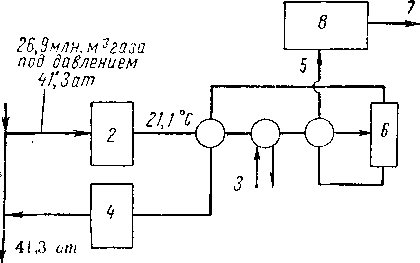
Рис. XV. 22. Принципиальная технологическая схема установки в г. Гринсберге, Кентукки [XV. 23; XV. 21].
I — газопровод; 2 — осушка; 3 — охлаждение этана (—71° С);
4 — компрессоры; 5 — жидкость + пары (—73° С, 10 ат); 6— сепаратор (—75,5° С, 37,5 ат)\ 7 — 1665 л3 в сутки этана, иропана, бутанов и более тяжелых углеводородов; 8 — се-парадионная установка.
Установка фирмы «Нейшнл петро-кемикалс корпорации» в Тусколе (штат Иллинойс) описана Старком [XV. 30]. Установка работает на газе, поступающем по трубопроводу фирмы «Панхендл истерн пайплайн ко,м-пани». В установкё применяются Два сорбента; гексан с температурой —23° С и минеральное масло с молекулярным весом 180.
Состав перерабатываемого и остаточного газа на деэтанизационной установке в Гринсберге [XV.21, XV.23]
|
Компонент | Мольная фракция | |
| сырье |
остаточный газ | |
|
Двуокись углерода....... |
0,0035 | 0,0032 |
| 0,0042 | 0,0044 | |
| Метан............. |
0,9392 | 0,9577 |
| Этан.............. |
0,0364 | 0,0292 |
| 0,0101 | 0,0046 | |
| Изобутан ............ | 0,0018 | 0,0005 |
| /i-Бутан............ |
0,0024 | 0,0004 |
| Пентаны........... |
0,0011 | 0,0000 |
| Гексаны............ |
0,0009 | 0,0000 |
| Гептаны и более тяжелые фракции | 0,004 |
0,0000 |
| Всего . . . | 1,0000 |
1,0000 |
В г. Кливленд (штат Огайо) построена установка для сжижения природного газа, используемого для покрытия потребностей в газе в периоды «пик» [XV. 9,
XV. 10, XV. 12]. Общие проблемы сжижения и обратной газификации рассмотрены в статье Лаверти и Эдмисте-ра (Laverty and Edmister) [XV. 216]. Кливлендская установка работала вполне удовлетворительно, но в результате разрыва резервуара во время сильного пожара была уничтожена [XV. 16]. Жидкий метан, несмотря на летучесть, обладает значительной скрытой теплотой. Будучи пролит на землю, он ведет себя, как и любая другая жидкость, хотя и сильно испаряется. Отсутствие стоков вокруг резервуара в Кливленде и послужило причиной больших разрушений во время пожара.
На установке применяли так называемый «каскадный процесс» сжижения газа с использованием в качестве охладителей этилена и аммиака (рис. XV. 23). При избыточном давлении 42 ат газ охлаждали до —95° С, затем в одной ступени снижали избыточное давление до 3,8 ат, а температуру до —139° С. После этого вновь в одной ступени снижали избыточное давление образовавшейся жидкости до 0,7 ат, а ее температуру до
— 161° С (т. е. до условий хранения). Для хранения сжиженного газа использовали стальные сферические резервуары с двумя концентрическими обечайками, пространство между которыми (0,9 м) было заполнено пробкой. Внутренний резервуар имел диаметр 17,1 м, он был изготовлен из стали с 3,5% Ni и 0,09% С (рис. XV. 23а). Один из таких двойных сферических резервуаров, заполненный сжиженным газом, уцелел и во время пожара.
Распространение более дешевого подземного хранения снизило интерес к сжижению как методу создания запасов газа на периоды «пик». Этому способствовало также и впечатление, произведенное пожаром, вызвавшим большие жертвы и разрушения.
Было предложено перевозить,сжиженный газ из мест добычи в пункты потребления [XV. 13, XV. 2, XV. 8а].
Например, высказывалась мысль о целесообразности перевозки сжиженного газа в танкерах из Венесуэлы на Атлантическое побережье США' [XV. 13]. Подсчеты показывают, что стоимость перевозок в танкерах (включая и расходы на сжижение газа) при больших расстояниях может быть меньшей по сравнению с транспортировкой по трубопроводу, при этом имеется возможность выбора любого маршрута.
Предложенные процессы сжижения природного газа показаны на рис. XV. 24 — XV. 26. С термодинамической точки зрения экспандер, показанный на рис. XV. 24, весьма рационален, его использование зависит от наличия машины, способной эффективно работать со смесью, содержащей большой процент жидкости. При расчете установок сжижения главная задача состоит в том, чтобы найти условия, обеспечивающие минимальную первоначальную стоимость установки и минимальные эксплуатационные расходы. Наиболее важной статьей оборудования подобных установок являются компрессоры, предназначенные для нагнетания циркулирующего несжижен-ного газа и охлаждающих средств. Для различных установок требуется мощность в 140—250 л. с. на 10 000 м3/сутки сырья. Как правило, минимальные первоначальные и эксплуатационные затраты получают при осуществлении процесса с меньшей установленной мощностью компрессоров.
При выборе теплообменников необходимо учитывать, что в данном случае теплообмен необходимо осуществлять с малой разницей температур [XV. 11, XV. 22]. Отложение гидратов в теплообменниках предотвращается изменением направления потока и специальной продувкой (рис. XV. 27).
При выборе материалов и изготовлении теплообменников используют' опыт, накопленный при производстве жидкого кислорода [XV. 21, XV. 22, XV. 11, XV. 4]. Материалами, обладающими необходимыми теплопроводностью и свойствами в условиях низких температур, яв-
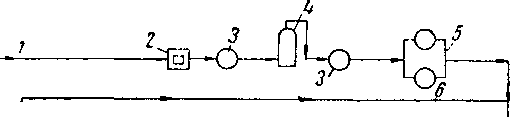
-1'С 15/С I -1°С ,7 ^2Sa{wpJrh02jgUn $
г*"'-!-' о \^8°h
-2/CirJ L
fig 7
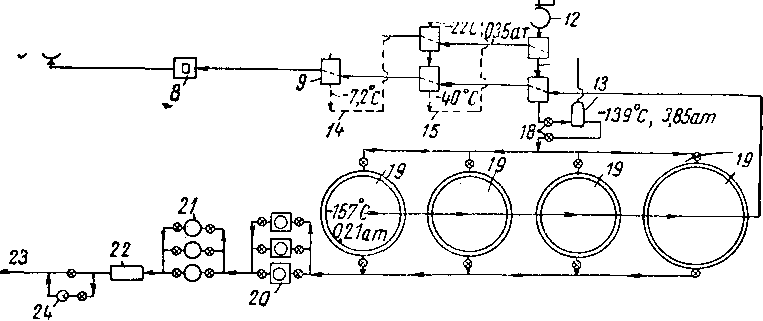
Рис. XV. 23. Схема установки сжижения природного газа в Кливленде [XV. 16].
/ — газ из газопровода (2,1 ат): 2 — компрессор
600 л. с. (42 ат); 3 — масляный сепаратор; 4 — удаление СО г моиоэтаноламииом и диэтиленгликолем; 5 ~
осушка активированной
окисью алюминия; 6 —
компрессор 1200 л, с.; 7—¦
рециркуляционный компрессор № 1 (800 л, с., 42 аг); 8 — рециркуляционный компрессор № 2 (150 л. с.); 9 — одноступенчатый теплообменник для газа; 10— конденсатор этилена; 11 — тея-лообменник (для метана и этилена); 12 — промежуточная емкость (—91° С, 42 ат)', 13— резервуар для первичной жидкости —139° С. 3,85 ат; 14 — система цир
куляции аммиака; 15 — Система циркуляции этилена;
16 ~ компрессор (500 л. с.);
17 — конденсатор аммиака с водным охлаждением; 18 — расширительные вентили;
19 — резервуары для хранения сжиженного природного газа (—157° С, 0,2 ат);
20 — насосы для жидкого газа; 21 — регазификация (острым газом); 22 — нагрев газа (мятым паром); 23 — газ потребителю; 24 — контрольный клапаи.
ляются алюминий и медь; обычно предпочитают применять алюминий, так как стоимость его меньше.
При сжижении природного газа большое внимание уделяется его осушке и очистке. Применением обычных методов осушки с твердыми поглотителями можно снизить влагосодержание газа практически до любого уровня. Все же наличие следов влаги может обусловить применение реверсивных теплообменников. В соответствии с расчетами, основанными на экстраполировании данных [XV. 15], при содержании менее 1,5% углекислоты в газе можно не опасаться образования твердой субстанции при рабочих давлениях, применяемых для сжижения. При атмосферном давлении растворимость двуокиси углерода в жидком метане составляет по данным Кона и Курата [XV. 21а] 0,2% мол.
При низких температурах обычная малоуглеродистая сталь становится хрупкой. Наоборот, аустенитные стали, изготовленные с добавкой никеля и других легирующих элементов, вполне удовлетворительно выдерживают действие низких температур.
Как свидетельствуют результаты ударных испытаний по Шарпи (Charpy), при низких температурах малоуглеродистые стали часто применяют для данной цели. Медь, алюминий и другие металлы типа «твердых растворов» при низких температурах не только не становятся хрупкими, но их прочность, наоборот, по мере снижения температуры может возрасти. Жаннис (Janis) [XV. 19] подготовил обзор 468 опубликованных в печати работ о поведении стали в условиях низких температур.
При решении вопросов хранения жидкого метана и других жидкостей при низких температурах можно частично воспользоваться опытом хранения жидкого кислорода и азота. Особое значение приобретает, естественно, теплоизоляция. Здесь наряду со старыми материалами (пробковыми блоками или пробковой крошкой) успешно применяют пенопласт и стекловату. Для предотвращения попадания влаги из воздуха в поры изоляции следует принимать различные меры. При охлаждении
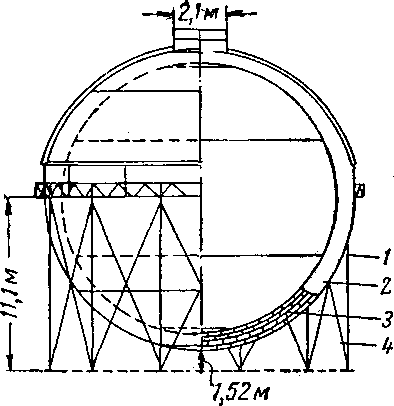
Рис. XV, 23а. Шарообразный резервуар для жидкого метана [XV. 16].
1 — вертикальные опоры (12); 2 — пробковая
крошка; 3 — пробковые блоки; 4 — рейки.
Все швы внутри и снаружи резервуаров должны быть выполнены стыковой сваркой. Внутренний резервуар должен быть изготовлен из нормализованной стали с содержанием 3*5 % Ni, прочие элементы конструкции — из малоуглеродистой стали. Диаметр внутреннего шара равен 17,4 м, наружного 19,9 м. Максимальная упругость паров 0,7 кГ/см2;. вес жидкого метана 418 кг/м3. Гидравлическое испытание при 125% рабочего напряжения в листах.
Максимальное рабочее напряжение в листах стенок резервуара 962 кГ/см2, емкость резервуара 2520 ма жидкости или 1580000 мъ газа; паровое пространство — 8—58% объема чистой жидкости*
Рис. XV. 24. Процесс Сжижения природного газа, предложенный Моррисоном [XV. 2J.
I — газовая скважина; 2 — сепаратор-классификатор; 3 — редукционный клапан; 4—- вода и конденсируемые компоненты;
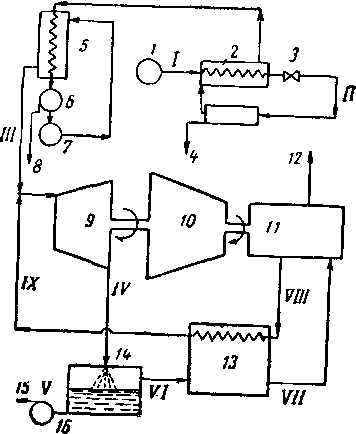
5 — теплообменник; в — аминовый абсорбер; 7 — осушитель (удаление воды); S —удаление СОг и т. г.; 9 — турборасшири-тельная машина (экспандер) для газа; 10 — паровая турбина;
II ¦—компрессоры, промежуточные и последующие холодильники; 12 — в паровой котел; 13 — предварительный Холодильник; 14 — сепаратор; 15 — а резервуар для жидкого газа; 16 —
насос.
| Место замера по рисунку | И | III | IV | V | |
|
Рабе. кГ/см*. . . t, *с..... ; ; ; Н, ккал/кг ....** | 175 26,7 185 | 73,5 — 17,8 179,4 |
70 — 13,2 185 | 1.0 — 161.5 103,3 | 1,0 — 161,5 10.5 |
| Место замера по рисуику | VI | VII | VIII | IX |
| Рабе. кПсм2 . и *с.......* ‘ • Н, ккал/кг . . , | 1.0 — 161 ,5 131,7 | 1,0 22,8 226,1 |
70 29,4 213,9 | 70 —70,5 117,7 |
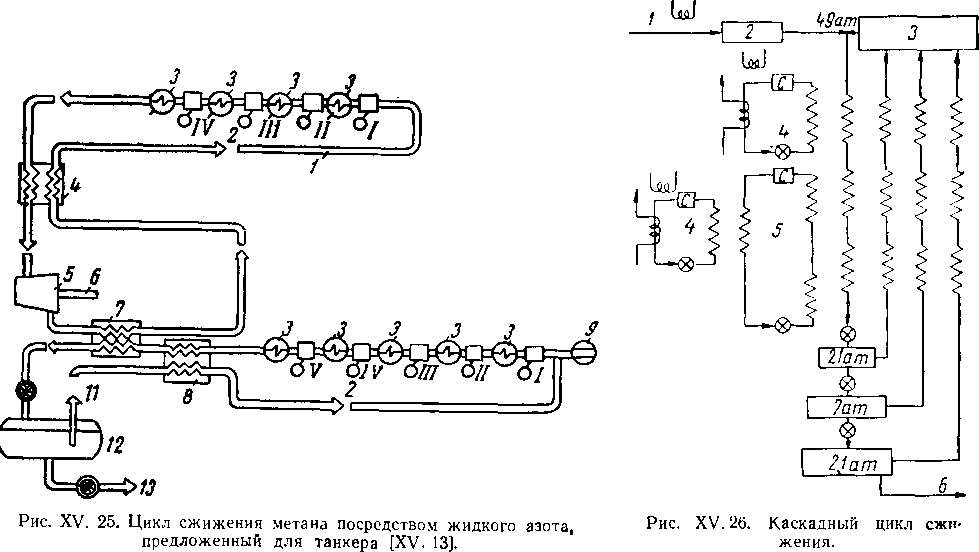
/ — азотный цикл; 2 — ступени; 3—промежуточные холодильники; 4 —> теплообменник А; 5 — расширительная машина; 6 — привод к компрессорам; / — теплообменник В; 8 — теплообменник С; 9— питание, 10— цикл охлаждения метана; 11 — отсекающий клапаи; 12 — емкость; 13 — жидкий метан в резервуары или в танкер.
1 — газ из скрубберов: 2 — расширитель
ная машина; 3 — компрессор с промежуточными холодильниками между ступеням ми; 4 — Фреон; 5 — этилен; 6 — жидкий метай.
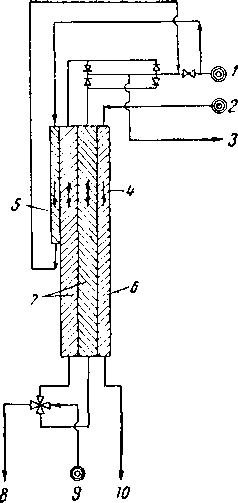
Рис. XV. 28. Приспособление танкера под перевозку жидкого метана [XV. 13].
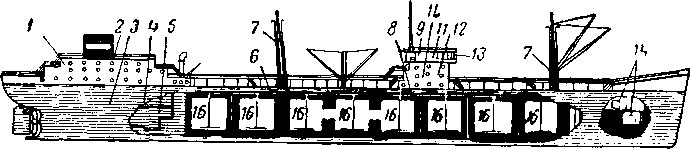
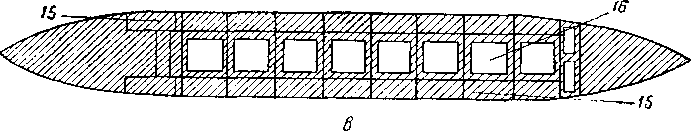
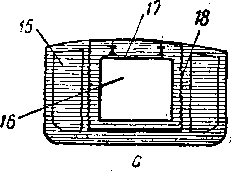
Рис. XV. 27. Направление потока в реверсивном теплообменнике [XV. 22].
I — азот; 2 — кнслород; 3 — холодный очищенный воздух; 4 — направления потока; 5 — проход для дополнительного охладителя (азота); 6 — проход для кислорода; 7 — реверсивные проходы для природного газа; 8 — продувочный азот; 9 — сырой воздух; 10 — чистый сухой кнслород.
а — продольный разрез; в — внутренний план танкера; с — поперечный разрез. 1 н 2 — жилые и подсобные помещения для команды; 3 — котельное отделение; 4 — машинное отделение; 5 — генераторное отделение; 6' — трубопроводы диаметром 4" для налива и отбора продуктов; 7 —свеча; 8 — насосное отделение для налива и отбора жидкого метана; 9 — штурманская рубка; 10 — радиорубка; —рулевое отделение; 12 — каюты; 15 — капитанский мостик; 14 — генератор инертного Газа; 15 — сохраненные наливные баки из нефтн; 16 — наливные баки для метана: 17 — изоляция из стирольного пенопласта («стирофоум») толщиной 300 мм; 18 — изоляция из стекловаты толщиной 75 мм.
резервуара, начиная с комнатной температуры до —150° С, происходит значительное сжатие. Это обстоятельство следует учесть при расчете резервуаров и обвязочных трубопроводов.
Если в резервуар с жидким газом попадает тепло, создается дополнительное давление. Это давление может возникнуть и в резервуарах, из которых удален весь жидкий метан. В одной из опубликованных работ [XV. 2] содержится рекомендация создавать из паров углекислоты в пустом резервуаре защитную среду сухого льда. Однако в данной рекомендации не учитывается то обстоятельство, что сухой лед растворим в жидком метане (в количестве 0,2% мол.), а при температуре—106° С упругость паров сухого льда очень невелика (0,001 мм рт. ст.). Чтобы получить упругость паров в 1 ат, сухому льду необходимо придать температуру -77° С.
Техника безопасности на установке сжижения природного газа должна быть более эффективной, чем на других предприятиях; необходимость этого продемонстрирована установкой в Кливленде. Все резервуары должны быть окружены сточными траншеями, способными вместить весь жидкий газ. Методы контроля за ведением процесса сжижения описаны в статье Руеманна (Ruhemann) [XV. 28]. Обычно используют устройства для понижения давления [XV. 32], автоматически включающиеся при повышении давления сверх допустимого. Но необходимо иметь достаточные гарантии, что эти устройства сработают в любых условиях. Для предотвращения разрыва установки в случае пожара может оказаться необходимой специальная система для быстрого сброса давления [XV. 33].
В регазификационной части установки (рис. XV. 23) жидкий метан подают насосами в теплообменники, обогреваемые паром. При этом необходимо принять меры для предотвращения утечки паров через сальники насосов.
Жидкий метан лучше всего перевозить в танкерах с наливными баками среднего объема, работающими при давлениях, лишь немного превышающих атмосферное. Использование таких танкеров имеет ряд преимуществ, в том числе и низкую стоимость перевозки [XV. 2, XV. 13]. На рис. XV. 28 показан проект реконструкции танкера типа Т-2 с целью использования его для перевозки наряду с нефтью жидкого метана.
В 1917 г. в США было освоено получение гелия из природного газа [XV. 29, XV. 35, XV. 1, XV. 24]. Установки по производству гелия принадлежат Горному бюро Министерства внутренних дел США. Завод в Ама-рильо (Техас), введенный в эксплуатацию в 1929 г., перерабатывает природный газ, содержащий около 1,8% гелия, 0,4% двуокиси углерода и 25% азота (остальную часть газа составляет в основном метан с примесью некоторого количества более тяжелых углеводородов).
Завод в Навахо (Нью-Мехико) перерабатывает газ, содержащий 7,8% гелия, 1,7% двуокиси углерода, 76% азота, остальная часть (14,5%) представляет собой газообразные углеводороды. Газ многих промыслов в Техасе— Панхендле и Канзасе содержит 0,3—0,4% гелия, но в состав таких газов обычно входит и азот в количестве, примерно в 10 раз превышающем содержание гелия.
Гелиевый завод в Амарильо первоначально практиковал удаление углекислоты раствором каустической соды; более современные заводы для этой цели (а также для осушки) применяют моноэтаноламин и диэтиленгликоль. Для окончательного удаления влаги используют активированную окись алюминия.
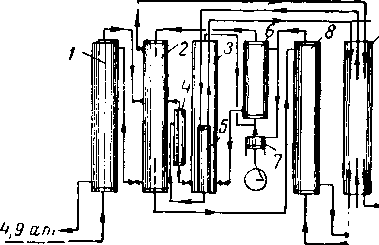
Процесс извлечения гелия описан Маллинсом (Mullins) [XV. 24] (рис. XV. 29). «Сырой» гелий, содержащий значительное количество азота, отделяют при низкой температуре от углеводородов. Эта сырая смесь гелия и азота поступает на сепарацию, одним из продуктов которой является чистый гелий. В процессе Маллинса газ пропускает через теплообменник 1, где он подвергается предварительному охлаждению и по существу, полному сжижению путем теплообмена с холодным переработанным газом, а затем дросселируется в комбинированный теплообменник-сепаратор 2, работающий при давлении около 14—21 кГ/см2. В сепараторе при данной температуре и давлении конденсируется природный газ примерно на 98%, а газовая фаза содержит около 60% гелия, 40% азота и очень небольшое количество метана. Холодные пары азота из вспомогательного охладительного цикла, который будет описан ниже, проходя вниз по трубам комбинированного теплообменника-сепаратора 2, обеспечивают некоторое охлаждение обеих фаз и ректификацию газовой фазы, что повышает содержание в ней гелия. Из сепаратора непрерывно раздельно извлекают жидкую и газовую фазы. Извлеченная газовая фаза—так называемый «сырой гелий» — проводится через теплообменник 9, где она нагревается до тем пературы, близкой к температуре воздуха, и затем по ступает для временного хранения в газгольдер низкого давления в ожидании дальнейшей очистки. Жидкая фаза из сепаратора дросселируется примерно до 4,9 кГ/см2 и проходит через теплообменник 1. Ее используют для охлаждения и сжижения поступающего газа. В процессе теплообмена сама жидкая фаза нагревается до температуры, близкой к температуре воздуха. Наконец, этот переработанный газ низкого давления повторно ком-примируется и возвращается в магистральный газопровод.
Первой ступенью очистки сырого гелия является ком-примирование его с давления, поддерживаемого в газгольдере, до 190 кГ/см2. Затем сырой гелий пропускают для осушки через кусковую каустическую соду, охлаждают без снижения давления в теплообменнике 9, где сырой гелий вступает в контакт с потоком холодного гелия из сепаратора 2, и наконец, подают в сепаратор 5 колонны 3. Сепаратор 5 погружен в «ванну» жидкого азота, поступающего из вспомогательного цикла сжижения азота. Ванна жидкого азота, находящаяся при атмосферном (или близком к нему) давлении, снижает температуру сырого гелия высокого давления почти до —180° С, в результате чего почти весь азот, находящийся в сыром гелии (а его там около 40%), переходит в жидкое состояние. Последним этапом очистки является непрерывное разделение двух фаз в сепараторе 5, откуда газовая фаза (технический гелий с чистотой около 98,5%) проходит через теплообменник 9 в газгольдеры высокого давления. Технический гелий можно подвергнуть дальнейшей очистке, пропуская его через активированный уголь при температуре—155-^185° С. В результате угольной сорбции чистота гелия повышается до 99,7% и выше. В прошлом гелий столь высокой чистоты выпускали лишь для специальных целей, но в настоящее время Горное бюро США принимает меры для организации массового производства гелия с чистотой до 99,99%. Имеется в виду подавать технический гелий из сепаратора 5 при температуре около —185°С в колонны, заполненные активированным углем, где холодный гелий обеспечит охлаждение активированного угля и будет освобожден от примесей в основном азота. Угольные очистители периодически будут реактивировать путем нагрева и очистки от азота в вакууме.
_ Сырой гелий, 1,05 ат ±^Г-190ат Технический гелий,190ат Дзот, 1fl5 ат
на очистку 9 активированным
углрм
Природный. газ,Ь2ат
Рис. XV. 29. Принципиальная схема завода по производству гелия [XV. 24].
/ — теплообменник для газа; 2 — сепаратор сырого гелия; 3 — колонна очистки гелия; 4 —* выработка жидкого азота; 5 — сепаратор чистого гелия; б —ожижитель азота; 7 — расширительная мпшииа; 8 — теплообменник для азота; 9 — теплообменник для гелия.
' 22,2 30 ЬО 50 60 70 SO 90 100 110 120 130 W 150 160 ПО 180 190 200 211
Знтальния, KK^jwz
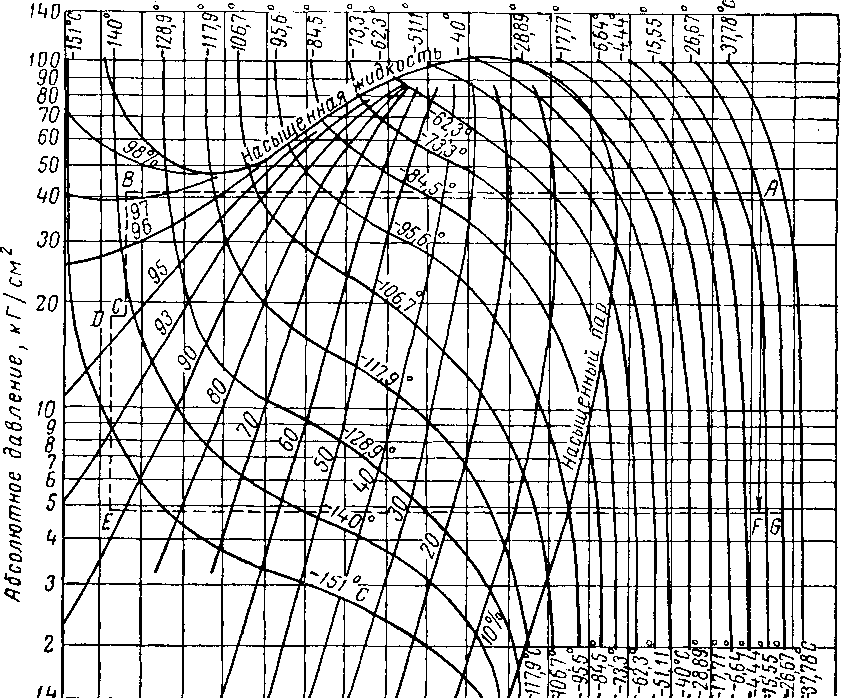
Рис. XV. 30. Цикл разделения сырого гелия иа диаграмме .давление — энтальпия [XV. 24].
Состав природного газа,%! гелий — 1,0% , азот — 16,3%, метан —71,4%, этан и более тяжелые углеводороды 11,3% .
Жидкий азот в сепараторе 5 содержит значительное количество растворенного в нем гелия, его дросселируют из сепаратора 5 в колонну 4, последняя работает при давлении сепаратора сырого гелия 2, с которым она соединена, что и обеспечивает выделение растворенного гелия путем снижения давления жидкости и извлечение гелия в сепараторе 2. Колонну 4 называют «вырабатывающей азот»; выходящий из нее жидкий азот дросселируется в колонну 3, где он обеспечивает надлежащее охлаждение сырого гелия и возмещает потерн жидкого азота в охлаждающей ванне. Жидкий азот содержит 95% и более азота, примесями являются небольшие количества метана и гелия.
Охлаждение в процессе получения гелия обеспечивается в основном расширением природного газа в системе циркуляции сырого гелия. Дальнейшее охлаждение, в том числе и до самых низких температур, создается вспомогательным циклом сжижения азота. В этом цикле азот компримируют в три ступени от давления, поддерживаемого в газгольдере, до 35—42 кГ/см2. Затем пропускают его через теплообменник 8 для предварительного охлаждения холодным выходящим азотом.
После этого поток азота разделяется, часть его поступает в ожижитель 6, а остаток экспандируется до давления, близкого к атмосферному, в экспандере 7.
Холодные пары азота из экспандера соединяются с парами азота из колонны очистки гелия 3 и проводятся через ожижитель 6, где они охлаждают и сжижают азот высокого давления. Затем холодные пары азота проводят через сепаратор сырого гелия 2 для ректификации этой гелиево-азотной смеси и охлаждения находящейся в сепараторе жидкой фазы и пропускают через теплообменник 8, охлаждая тем самым поступающий в цикл сжижения азот высокого давления. Жидкий азот, образовавшийся в ожижителе 6 при давлении 35—¦ 42 кГ/см2, дросселируется почти до атмосферного давления в гелиеочистителе 3 с целью поддержания необходимого уровня жидкого азота в охладительной ванне этой колонны.
Процесс разделения сырого гелия показан линией ABCDEG на диаграмме давление—энтальпия гелийсодержащего природного газа (рис, XV. 30).
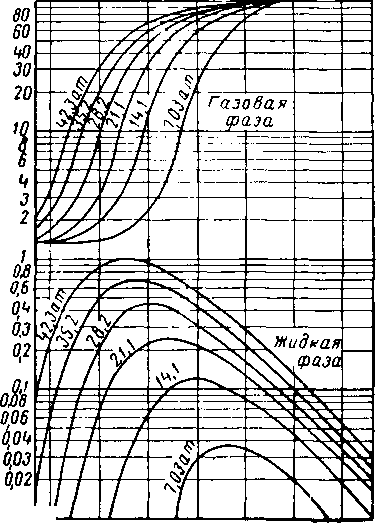
Содержание гелия в разделяемых фазах представлено на рис. XV. 31.
8^5-90 -ПО -130 -150 -170 -190 -210-216 . Температура,0 С
001U!
' Мольная концентрация гелия
Несколько заводов, принадлежащих Горному бюро, перерабатывают природный газ на пути его к потребителям. Может оказаться более экономичным перерабатывать газ со средним содержанием гелия (0,5—1,0%), чем газ, более богатый гелием. Повышенное содержание гелия обычно предполагает наличие большего количества азота, что делает остаточный газ бесполезным как топливо.
§ 5. ОЧИСТКА ПРИРОДНОГО ГАЗА ОТ АЗОТА
-84,5-30 -но
W0
Газы некоторых месторождений, особенно Панхендл и Хьюготон, содержат большое количество азота (10% и более, иногда до 30—35%). Чтобы исключить транспортировку больших количеств инертного газа на значительные расстояния, была изучена возможность удаления азота путем низкотемпературной переработки [XV. 25]. Наиболее логичным процессом в данном случае является сжижение. Необходимые условия для разделения фаз вытекают из свойств системы метан — азот. Была построена соответствующая полузаводская установка и проведены инженерные изыскания по процессу сжижения, но в промышленном масштабе еще процесс не был применен.
Рис. XV. 31. Содержание гелия в газовой и жидкой фазе типичного гелийсодержащего природного газа [XV. 24].
Состав природного газа. %: гелий — 1,4, азот—12,7, метан — 78,2, этан и более тяжелые углеводороды — 7,7,